题目内容
5.X元素原子的质量数为m,核内中子数为n,则X+的核外电子数为( )| A. | m-n | B. | m+n | C. | m-n-1 | D. | m-n+1 |
分析 先根据质子数=质量数-中子数计算质子数,再根据阳离子中核外电子数=质子数-电荷数计算一个阳离子含有的电子数.
解答 解:X元素原子中含有的质子数=质量数-中子数=m-n,x+中核外电子数=质子数-电荷数=m-n-1;
故选C.
点评 本题考查阳离子中核外电子数的计算,难度不大.要注意核素的相对原子质量在数值上等于其质量数.

练习册系列答案
相关题目
13.某无色混合气体可能由CH4(天然气的主要成分)、NH3、H2、CO、CO2和HCl中的某几种气体组成,在恒温恒压条件下,将此混合气体通过浓硫酸时,总体积基本保持不变;通过过量的澄清石灰水,未见变浑浊,但混合气体的总体积减小;把剩余气体导出后,在氧气中能够点燃,燃烧产物不能使硫酸铜粉末变色.则原混合气体中肯定含有( )
| A. | CO、HCl | B. | NH3、CO、HCl | C. | CH4、NH3、CO | D. | CH4、H2、CO、CO2 |
20.下列原子中,最难形成离子的是( )
| A. | 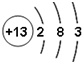 | B. |  | C. |  | D. |  |
10.电解水生成氢气和氧气这一事实说明( )
| A. | 水是由氢气和氧气组成的 | |
| B. | 水是由2个氢原子和1个氧原子构成的 | |
| C. | 水是由2个氢元素和1个氧元素组成的 | |
| D. | 水是由氢元素和氧元素组成的 |
17.现有盐酸、新制氯水、NaCl溶液和NaOH溶液,可用一种试剂将它们一一区别开,该试剂是( )
| A. | AgNO3溶液 | B. | 酚酞试液 | C. | 紫色石蕊试液 | D. | 饱和NaCl溶液 |
14.NA为阿伏加德罗常数的数值,下列说法中正确的是( )
| A. | 在密闭容器中加入1.5 mol H2和0.5 mol N2,充分反应后可得到NH3分子数为NA | |
| B. | 一定条件下,2.3 g的Na完全与O2反应生成3.6 g产物时失去的电子数为0.1NA | |
| C. | 1.0 L的0.1 mol•L-1Na2S溶液中含有的S2-数为0.1NA | |
| D. | 标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA |
15.以下能级符号正确的是( )
| A. | 5s | B. | 2d | C. | 3 f | D. | 1p |