题目内容
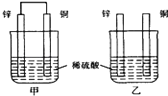
【题目】将纯锌片和纯铜片按图方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是
A. 两烧杯中铜片表面均无气泡产生
B. 甲中铜片是正极,乙中铜片是负极
C. 两烧杯中溶液的pH均增大
D. 甲、乙溶液均变蓝色
【答案】C
【解析】试题分析:A.甲中形成铜锌原电池,锌作负极,失电子,铜作正极,H+在铜极上得电子,生成H2,所以甲中铜片表面有气泡产生,乙池中锌直接与稀硫酸发生化学反应,在锌片上产生氢气,A项错误;B.乙中不能构成原电池,铜片不是电极,B项错误;C.甲乙两烧杯反应的总方程式都为Zn+H2SO4=ZnSO4+H2↑,溶液中硫酸的浓度降低,溶液的PH增大,C项正确;D.根据上述分析,铜片不参与反应,所以甲、乙溶液不会变蓝,D项错误;答案选C。

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
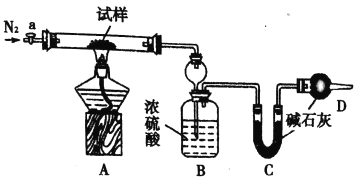
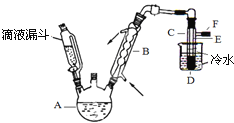
【题目】下图是实验室用乙醇、硫酸、溴化钠混合反应来制备溴乙烷的装置。反应需要加热,图中省去了加热装置。乙醇、溴乙烷、溴的有关性状参数见下表。
乙醇 | 溴乙烷 | 溴 | |
状态 | 无色液体 | 无色液体 | 深红棕色液体 |
密度/g.cm-3 | 0.79 | 1.44 | 3.1 |
沸点/℃ | 78.5 | 38.4 | 59 |
水溶性 | 易溶 | 难溶 | 微溶 |
(1)加热A中三种反应物的混合物时,发生反应的化学方程式为: 。
(2)若选用较浓的硫酸作为反应物,得到的产品则会呈棕黄色,这说明反应过程中有 生成。为去除颜色,最好选择下列的 溶液来洗涤产品。
A.四氯化碳 B.硫酸钠 C.碘化亚铁 D.亚硫酸钠
产品选择上述溶液洗涤后,还需再用蒸馏水洗涤一次。洗涤液与产品分离的方法是 (填方法名称)。
(3)装置中,B和D两部分的作用分别是:B ;D 。