题目内容
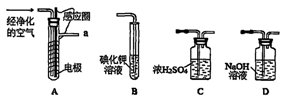
氧化二氯是黄棕色具有强烈刺激性的气体。它的熔点-116℃,沸点3.8℃.氧化二氯不稳定,接触一般有机物易爆炸;它易溶于水(1∶100)同时反应生成次氯酸溶液。制取少量氧化二氯,是用干燥的氧化汞与氯气反应(还生成HgO·HgCl2)。装置如图,仅铁架台和夹持仪器已略去。
部分物质的有关物理数据如下:
| 化学式 | 熔点(单位:℃) | 沸点(单位:℃) |
| N2 | -209.86 | -195.8 |
| O2 | -218.4 | -183 |
| CO2 | -57 | / |
| NH3 | -77.3 | -33.35 |
| Cl2 | -101 | -34.6 |
试回答:
(1)A中深色固体与无色液体制备气体的离子方程式: 。
(2)B中盛有液体c是饱和 ,C中的液体d是浓硫酸。?
(3)氧化二氯制备出之后,要冷却为固态才便于操作和贮存,则E中的保温瓶中盛有致冷剂,它应是
(在干冰、冰水、液态空气、液氨中选择)。在E的内管得到的Cl2O中可能含有的主要杂质是反应物中过量的 。
(4)装置D、E间的连接方式与A、B、C间的连接方式有明显的区别,这区别是D、E中无 管、塞,用这些不同的连接方式的主要理由是氧化二氯接触有机物而 。
(12分)(1)a:2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O; (2) 饱和NaCl溶液
(3)液态空气 Cl2 (4)橡胶 爆炸
解析试题分析:(1)由装置图可知,A中发生反应制备氯气,反应不需加热,深色固体试剂a与溶液b反应,通常应为高锰酸钾与浓盐酸,反应的离子方程式为2MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O。
(2)HCl易挥发,A中生成的氯气中含有HCl、H2O,用饱和食盐水吸收HCl,用浓硫酸干燥,先除氯化氢,后干燥,故B中盛有液体c是试剂饱和食盐水。
(3)由题目信息可知,氧化二氯气体的熔点-116℃,熔点很低,所以根据表中数据可知,应该选择沸点很低的液态空气进行制冷;根据工艺流程可知,D中反应氯气可能不能成分反应,由于氯气易液化,所以E的内管得到的氧化二氯中可能含有杂质是液氯。
(4)由信息可知,氧化二氯不稳定,接触一般有机物易爆炸,因此 Cl2O不能与有机物接触,所以A、B、C间用乳胶管连接,D、E间不能乳胶管连接。
考点:考查物质制备实验方案设计与评价的有关判断

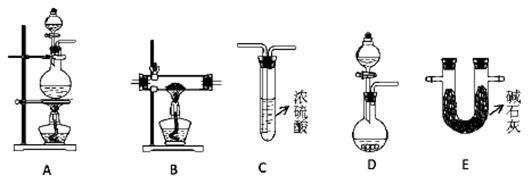
某实验小组利用如下装置(部分固定装置略)制备氮化钙(Ca3N2),并探究其实验式。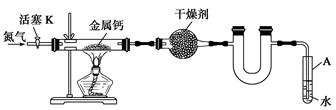
(1)反应过程中末端导管必须始终插入试管A的水中,目的是_____________________。
(2)制备氮化钙的操作步骤是:
①打开活塞K并通入N2;
②点燃酒精灯,进行反应;
③反应结束后,__________________________________________________________;
④拆除装置,取出产物。
(3)数据记录如下:(假设反应完全)
| 空硬质管质 量m0/g | 硬质管与钙的 质量m1/g | 硬质管与产物 的质量m2/g |
| 14.80 | 15.08 | 15.15 |
① 计算得到实验式CaxN2,其中x=________。
②若通入的N2中混有少量O2,请比较x与3的大小,并给出判断依据:
______________________________________________________________________。


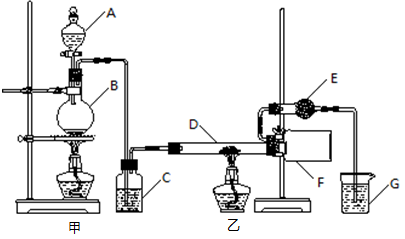
 2O3)。
2O3)。