题目内容
Fe与稀HNO3反应时,若两者消耗物质的量之比为4∶10,且生成 Fe(NO3)2,则反应中生成的还原产物可能是( )
| A.N2 | B.N2O | C.NO | D.NH4NO3 |
BD
试题分析:硝酸与金属反应时硝酸部分被还原,假设Fe有4mol,则未被还原的硝酸为8mol,因此被还原的硝酸有2mol,4molFe在反应中失去8mol电子,所以2mol硝酸得8mol电子,这其中可以是2mol硝酸均得电子,也可以是1mol硝酸得1mol硝酸不得,因此硝酸的还原产物可能为N2O,也可能是NH4NO3。答案选BD。
点评:本题的关键就是要分析出得电子后的平均化合价,否则会漏选。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 2NO。该反应中,氧化剂是________(填化学式),若反应中消耗了1 mol N2,则转移_______mol电子。
2NO。该反应中,氧化剂是________(填化学式),若反应中消耗了1 mol N2,则转移_______mol电子。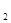 O,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是
O,则该反应中被还原的硝酸与未被还原的硝酸的物质的量之比是 、ClO
、ClO ;三种含氯元素的离子,其中C1O
;三种含氯元素的离子,其中C1O



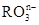 和氟气可发生如下反应:
和氟气可发生如下反应: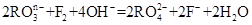 ,从而可知在
,从而可知在 ,若反应后
,若反应后 变成
变成 ,且反应中氧化剂与还原剂的离子个数比为5:2,则R2O8n-中R元素的化合价以及n分别为
,且反应中氧化剂与还原剂的离子个数比为5:2,则R2O8n-中R元素的化合价以及n分别为