题目内容
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是
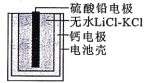
A. Ca为正极 B. 放电过程中,Li+向负极移动
C. 每转移0.2mol电子,理论上生成20.7gPb D. 电池工作一段时间后,正极质量增大
【答案】C
【解析】A、由原电池总反应可知Ca化合价升高,失电子,故Ca为原电池的负极,故A错误;B、电池工作时,阳离子向正极移动,故B错误;C、根据电池总反应,每反应1molCa转移2mol电子,正极生成1molPb,每转移0.2mol电子,理论上生成0.1molPb,即20.7gPb,故C正确;D、电池工作时,正极为PbSO4固体转化为Pb固体,正极质量减小,故D错误。故选C。

练习册系列答案
相关题目