题目内容
【题目】100mL氯化镁和氯化铝的混合溶液,其中c(Mg2+)为0.2mol·L-1,c(Cl-)为1.3mol·L-1。要使Mg2+全部转化为沉淀分离出来,至少需加2mol·L-1NaOH溶液的体积为
A. 40mL B. 72mL C. 80mL D. 128mL
【答案】C
【解析】
溶液中n(Cl-)=0.1L×1.3mol/L=0.13mol,溶液中n(Mg2+)=0.2mol/L×0.1L=0.02mol,
根据电荷守恒,溶液中3n(Al3+)+2 n(Mg2+)= n(Cl-),n(Al3+)=![]() =0.03mol,将100mL此溶液中的Mg2+转化为Mg(OH)2沉淀并分离析出,氢氧化钠一定过量,铝离子全部转化为AlO2-,所以反应后溶液为NaCl、NaAlO2的混合液,由原子守恒可知n(NaOH)=n(Na)=n(Cl)+n(Al)=0.13mol+0.03mol=0.16mol,所以至少需要2mol/L氢氧化钠溶液的体积为
=0.03mol,将100mL此溶液中的Mg2+转化为Mg(OH)2沉淀并分离析出,氢氧化钠一定过量,铝离子全部转化为AlO2-,所以反应后溶液为NaCl、NaAlO2的混合液,由原子守恒可知n(NaOH)=n(Na)=n(Cl)+n(Al)=0.13mol+0.03mol=0.16mol,所以至少需要2mol/L氢氧化钠溶液的体积为![]() =0.08L=80mL,故C正确,
=0.08L=80mL,故C正确,
故选C。

【题目】某小组同学欲研究SO2的性质。
(1)将相关的含硫物质分为如下表所示3组,第2组中物质X的化学式是________。
第1组 | 第2组 | 第3组 |
S(单质) | SO2、X、Na2SO3、NaHSO3 | SO3、H2SO4、Na2SO4、NaHSO4 |
(2)利用下图所示的装置研究SO2的性质:(熔点:SO2 -76.1 ℃,SO3 16.8 ℃;沸点:SO2 -10 ℃,SO3 45 ℃)
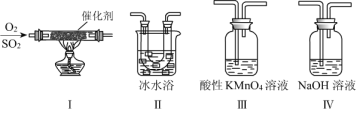
①装置Ⅰ模拟工业生产中SO2催化氧化的反应,其化学方程式是__________________。
②甲同学按Ⅰ、Ⅱ、Ⅲ、Ⅳ的顺序连接装置,装置Ⅱ的作用是_____________________;装置Ⅳ的作用是_________________。
③装置Ⅲ中溶液逐渐褪色,说明SO2具有__________性