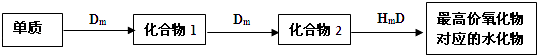
题目内容
【题目】如图所示装置中,X是铁,Y是石墨电极,a是硫酸钠溶液,实验开始前, 在U形管的两边同时各滴入几滴酚酞试液,下列叙述正确的是( )
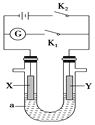
A. 闭合K1,断开K2,X极放出H2
B. 闭合K1,断开K2,Y极为阳极
C. 闭合K2,断开K1,Y极的电极反应式为O2+2H2O+4e-===4OH-
D. 闭合K2,断开K1,工作一段时间后,X电极附近显红色
【答案】D
【解析】A项,闭合K1,断开K2,形成原电池,X(铁)作负极,失电子发生氧化反应生成Fe2+,故A错误;B项,闭合K1,断开K2,形成原电池,Y(石墨)为正极,故B错误;C项,闭合K2,断开K1,形成电解池,Y是阳极,OH-失电子发生氧化反应,故C错误;D项,闭合K2,断开K1,形成电解池,X是阴极,电极反应式可表示为:2H2O+2e-=H2+2OH-,所以工作一段时间后,X电极附近显红色,故D正确。

 阅读快车系列答案
阅读快车系列答案【题目】炼锌厂的铜镉废渣中含有铜、锌、镉、铁、砷等元素,其含量依次减少。对这些元素进行提取分离能减少环境污染,同时制得ZnSO47H2O实现资源的再利用。其流程图如下。已知FeAsO4难溶于水;ZnSO47H2O易溶于水,难溶于乙醇。

金属离子 | Fe3+ | Zn2+ | Mn2+ | Cu2+ | Cd2+ |
开始沉淀pH | 2.7 | 6.5 | 7.7 | 5.2 | 6.9 |
沉淀完全pH | 3.2 | 8.0 | 9.8 | 6.4 | 9.4 |
请回答下列问题:
(1)提高浸出率可以采用的方法是(写出其中一点即可)______________。
(2)滤液I中有少量的AsO33-,AsO33-与Cd反应会产生一种有毒氢化物气体,该气体的分子式为_________。向滤液I中滴入酸性KMnO4溶液可发生如下反应,完成该反应的离子方程式:____Fe2++___AsO33-+___MnO4-+___□=___Mn2++___FeAsO4↓+___□,
_________________________,判断该滴定终点的现象是_____________________________________。
(3)流程中②调节pH时可以选用的试剂为__________,滤渣Ⅱ的主要成份为________。
(4)制得的ZnSO47H2O需洗涤,洗涤晶体时可选用试剂为(________)。
A.水 B.乙醇 C. 饱和硫酸锌溶液 D.稀硫酸