题目内容
10.10mL 0.5mol/L NaNO3溶液和10mL 0.5mol/L CaCl2溶液混合后,混合液中Cl-浓度为(假设溶液体积混合前后不变)( )| A. | 0.5mol/L | B. | 0.6mol/L | C. | 1mol/L | D. | 2mol/L |
分析 混合前后后溶液中氯离子物质的量不变,根据稀释定律计算混合液中Cl-浓度.
解答 解:混合前后后溶液中氯离子物质的量相等,则:
0.01L×0.5mol/L×2=c混合(Cl-)×0.02L
解得c混合(Cl-)=0.5mol/L,
故选:A.
点评 本题考查物质的量浓度有关计算,比较基础,注意对定义式的理解与灵活应用.

练习册系列答案
相关题目
1.有四位同学分别对四种溶液中所含的离子进行检测,结果如下,其中错误的是( )
| A. | Ca2+、HCO3-、Cl-、K+ | B. | OH-、CO32-、Cl-、K+ | ||
| C. | Ba2+、Na+、OH-、NO3- | D. | Cu2+、NO3-、OH-、Cl- |
5.下列关于化学反应的相关描述不正确的是( )
| A. | 胃舒平中含有氢氧化铝,可治疗胃酸过多:Al(OH)3+3HCl═AlCl3+3H2O | |
| B. | 碳铵是一种常用化肥,60℃分解完全:2NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+CO2↑+H2O↑ | |
| C. | 生石灰可用作建筑材料:CaO+H2O=Ca(OH)2,属于化合反应 | |
| D. | 实验室常用氧化还原反应制备氧气:2H2O2 $\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑ |
15.可逆反应:3X(g)?3Y(?)+Z(?)△H<0,随着温度的降低,气体的平均相对分子质量有变小的趋势,则下列判断正确的是( )
| A. | Y和Z可能都是气体 | B. | Y和Z可能都是固体 | ||
| C. | 若Z为固体,则Y一定是气体 | D. | Y和Z一定是气体 |
2.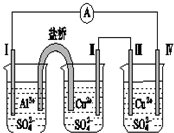 某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )
某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )
 某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )
某同学 用 如图所示的电化学装置 电解硫酸铜溶液,有一个电极为Al,其它三个电极均为Cu,则 下列说法正确的是( )| A. | 电子方向:电极Ⅳ→→电极Ⅰ | B. | 电极Ⅰ发生还原反应 | ||
| C. | 电极Ⅱ逐渐溶解 | D. | 电极Ⅲ的电极反应:Cu-2e-═Cu2+. |
19.下列事实与胶体性质无关的是( )
| A. | 明矾净水 | |
| B. | 卤水点豆腐 | |
| C. | 三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 | |
| D. | 阳光透过茂密的树林所产生的美丽光线 |