题目内容
下列说法中错误的是( )
| A、根据对角线规则,铍和铝的性质具有相似性 |
| B、在H3O+、NH4+和[Cu(NH3)4]2+中都存在配位键 |
| C、CH2=CH2中的C原子和BF3中的B原子均为sp2杂化 |
| D、P4和CH4都是正四面体分子且键角都为109°28ˊ |
考点:配合物的成键情况,键能、键长、键角及其应用,原子轨道杂化方式及杂化类型判断
专题:化学键与晶体结构
分析:A.元素周期表中,某些主族元素与右下方的主族元素(如图)的性质具有相似性,这种规律被称为“对角线规则”,根据元素的位置情况来判断;
B.在物质或离子中中心原子含有空轨道,和含有孤电子对的原子或离子能形成配位键,在H3O+、NH4+和[Cu(NH3)4]2+中都存在配位键;
C.根据杂化轨道数判断杂化类型,杂化轨道数=δ键数+孤对电子对数,据此判断杂质类型;
D.P4和CH4都是正四面体分子,CH4键角为109°28ˊ,P4键角为60°.
B.在物质或离子中中心原子含有空轨道,和含有孤电子对的原子或离子能形成配位键,在H3O+、NH4+和[Cu(NH3)4]2+中都存在配位键;
C.根据杂化轨道数判断杂化类型,杂化轨道数=δ键数+孤对电子对数,据此判断杂质类型;
D.P4和CH4都是正四面体分子,CH4键角为109°28ˊ,P4键角为60°.
解答:
解:A.对角线规则为:沿周期表中金属与非金属分界线方向对角的两主族元素性质相似,铍和铝位置关系符合对角线规则,物质的性质相似,故A正确;
B.H3O+中O提供孤电子对,H+提供空轨道,二者形成配位键,氨气分子中氮原子含有孤电子对,氢离子提供空轨道,可以形成配位键,NH4+含有配位键,铜原子提供空轨道,氮原子提供孤电子对,[Cu(NH3)4]2+中存在配位键,故B正确;
C.C2H4中C原子杂化轨道数=δ键数+孤对电子对数=3+0=3,所以采取sp2杂化,B原子杂化轨道数=δ键数+孤对电子对数=3+0=3,所以采取sp2杂化,故C正确;
D.CH4中中心原子价层电子对个数为4,为四面体结构,4个共价键完全相同,为正四面体且键与键之间夹角为109°28′,P4 结构为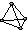 ,为正四面体结构,键与键之间夹角为60°,故D错误;
,为正四面体结构,键与键之间夹角为60°,故D错误;
故选D.
B.H3O+中O提供孤电子对,H+提供空轨道,二者形成配位键,氨气分子中氮原子含有孤电子对,氢离子提供空轨道,可以形成配位键,NH4+含有配位键,铜原子提供空轨道,氮原子提供孤电子对,[Cu(NH3)4]2+中存在配位键,故B正确;
C.C2H4中C原子杂化轨道数=δ键数+孤对电子对数=3+0=3,所以采取sp2杂化,B原子杂化轨道数=δ键数+孤对电子对数=3+0=3,所以采取sp2杂化,故C正确;
D.CH4中中心原子价层电子对个数为4,为四面体结构,4个共价键完全相同,为正四面体且键与键之间夹角为109°28′,P4 结构为
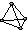 ,为正四面体结构,键与键之间夹角为60°,故D错误;
,为正四面体结构,键与键之间夹角为60°,故D错误;故选D.
点评:本题较为综合,考查了对角线规则、配位键、原子杂化类型的判断、键角等知识,根据“杂化轨道数=δ键数+孤对电子对数”来解答原子杂化问题,根据价层电子对互斥理论判断晶体结构及键角,注意配位键形成的条件,题目难度中等.

练习册系列答案
相关题目
现有①Al2(SO4)3 ②Cu(NO3)2 ③Ba(OH)2 ④NH4Cl ⑤NaNO3五种溶液,不用其它试剂能将一一鉴别出来的顺序是( )
| A、①②③④⑤ |
| B、②③④①⑤ |
| C、②④③①⑤ |
| D、②⑤③①④ |
下列各组失去标签的溶液,不另加其他试剂(仅利用组内物质间的反应),运用试管和胶头滴管就能区别开来的是( )
| A、FeCl3、NaOH、KSCN、Ba(NO3)2 |
| B、NaCl、Na2CO3、KNO3、HCl |
| C、BaCl2、Na2SO4、NaOH、NaCl |
| D、Na2SO4、BaCl2、K2CO3、KNO3 |
下列说法不正确的是( )
| A、盛有被KCl饱和溶液浸泡过的琼脂的U型管,可用作原电池的盐桥 |
| B、Al3+能水解为Al(OH)3胶体,明矾可用作净水剂 |
| C、甲醛能使蛋白质变性,可用作食品防腐剂 |
| D、在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 |
短周期元素M、W、X、Y、Z的原子序数依次增大,M元素的一种核素没有中子,且M、W、X、Y+、Z的最外层电子数与其电子层数的比值依次为1、2、3、4、2(不考虑零族元素).下列关于这些元素的叙述正确的是( )
| A、X分别和其它四种元素均可形成至少2种化合物 |
| B、M分别和W、X、Y、Z形成化合物,均显相同化合价 |
| C、M、X、Z三种元素组成的化合物含有离子键 |
| D、M、X、Y组成化合物和Y、Z组成化合物,其等物质的量浓度的水溶液中由水电离出的氢离子浓度相同 |
①在含有FeCl3和BaCl2的酸性混合液中,通入足量SO2气体,有白色沉淀生成,过滤后,向滤液中滴加KSCN溶液,不出现红色,②在氨水和BaCl2的混合液中,通入适量SO2气体,也有白色沉淀生成,由此得出的结论是( )
| A、白色沉淀都是BaSO3 |
| B、①白色沉淀是BaSO3和S,②是BaSO3 |
| C、①白色沉淀是BaSO4,②是BaSO3 |
| D、①白色沉淀是FeSO3,②是BaSO3 |
下列有关说法正确的是( )
| A、铅蓄电池在放电时,两极质量均增加 | ||
| B、钢铁在中性溶液中主要发生析氢腐蚀 | ||
| C、在室温下能自发进行的反应,其△H一定小于0 | ||
D、0.1mol?L-1 Na2S溶液加水稀释时,
|
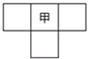 甲、乙、丙、丁为4种短周期元素.甲与乙、丙、丁在周期表中的位置关系如图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24.下列判断正确的是( )
甲、乙、丙、丁为4种短周期元素.甲与乙、丙、丁在周期表中的位置关系如图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24.下列判断正确的是( )| A、甲、乙、丙、丁四种元素的简单气态氢化物中,乙的简单气态氢化物最稳定 |
| B、甲、乙、丙、丁四种元素的常见单质都是无色的 |
| C、由甲元素和丁元素组成的两种常见化合物的分子都是极性分子 |
| D、甲、乙、丙、丁四种元素的简单阴离子半径从大到小顺序为:丁>乙>丙>甲 |
 近年来,由于温室效应和资源短缺等问题,关于CO2和碳酸盐应用的研究受到人们的重视.某研究小组利用反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,制备CO2与H2 的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用.
近年来,由于温室效应和资源短缺等问题,关于CO2和碳酸盐应用的研究受到人们的重视.某研究小组利用反应:CO(g)+H2O(g)?H2(g)+CO2(g)△H=-41.2kJ/mol,制备CO2与H2 的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用.