题目内容
若NA表示阿伏加德罗常数,下列说法正确的是
| A.含有NA个氖原子的氖气在标准状况下的体积约为11.2L |
| B.2.3gNa被O2完全氧化时,失去电子数为0.1NA |
| C.2Llmol/L的盐酸中所含氯化氢分子数约为2NA |
| D.标准状况下,5.6LCCl4含有的分子数为0.25NA |
B
解析试题分析:A、氖分子是由1个氖原子构成的,所以含有NA个氖原子的氖气是1mol,在标准状况下的体积约为22.4L,A不正确;B、钠是第IA族元素,在反应中失去1个电子。2.3g钠的物质的量是0.1mol,因此2.3gNa被O2完全氧化时,失去电子数为0.1NA,B正确;C、氯化氢是强电解质,溶于水完全电离出氯离子与氢离子,因此在盐酸溶液中不存在氯化氢分子,C不正确;D、标准状况下,四氯化碳不是气态,不能适用于气体摩尔体积,则标准状况下5.6LCCl4含有的分子数一定不是0.25NA,D不正确,答案选B。
考点:考查阿伏伽德罗常数的计算

练习册系列答案
 考前必练系列答案
考前必练系列答案
相关题目
下列叙述中指定粒子数目一定大于NA的是
| A.11.2L氧气和臭氧的混合气体所含的原子数 |
| B.1mol CaC2固体中含阴离子总数 |
| C.1L1mol/LCH3COOH溶液中所含分子总数 |
| D.1molCl2参加化学反应获得的电子数 |
据某权威刊物报道,科学家在宇宙中发现了H3分子,对于相同物质的量的H3和H2,下列各项中一定相等的是( )
| A.质量 | B.体积 | C.分子数 | D.原子数 |
下列有关化学用语表示正确的是
A.-CHO的电子式: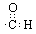 |
B.丙烷分子的比例模型为: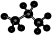 |
C.2-乙基-1,3-丁二烯的键线式: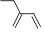 |
D.邻羟基苯甲酸的结构简式: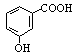 |
设NA为阿伏伽德罗常数的值。下列说法正确的是( )
| A.标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
| B.常温常压下,18g H2O含有的原子总数为3NA |
| C.标准状况下,11.2L酒精(CH3CH2OH)中含有分子的数目为0.5NA |
| D.常温常压下,1 mol硫酸钾中阴离子所带电荷数为NA |
碘值是指100 g油脂中所能吸收(加成)碘的克数。测得某植物油碘值为a g,以NA表示阿伏加德罗常数,则b g该植物油中含有的碳碳双键数为
| A.abNA/25400 | B.abNA/12700 | C.abNA/2.54 | D.abNA/1.27 |
下列叙述中正确的是( )
| A.1 mol H2O的质量是18g/mol | B.硫酸根离子的摩尔质量是96g |
| C.CO2的摩尔质量是44g/mol | D.HCl的相对分子质量是36.5g/mol |
利用碳酸钠晶体(Na2CO3·10H2O)来配制0.5 mol/L的碳酸钠溶液1 000 mL,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是( )
| A.称取碳酸钠晶体100 g |
| B.定容时俯视刻度线 |
| C.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗 |
| D.定容后,将容量瓶振荡均匀,静置发现液面低于刻度线,于是又加入少量水至刻度线 |
下表为四种溶液的溶质质量分数和物质的量浓度的数值,根据表中数据判断四种溶液中密度最小的是( )。
| 溶液 | KOH | HNO3 | CH3COOH | HCl |
| 溶质质量分数w(%) | 56 | 63 | 60 | 36.5 |
| 物质的量浓度c(mol·L-1) | 14.3 | 13.8 | 10.6 | 11.8 |
A.HCl B.HNO3 C.CH3COOH D.KOH