题目内容
多硫化钠Na2Sx(x≥2)在结构上与Na2O2、FeS2等有相似之处,Na2Sx在碱性溶液中可被NaClO氧化成Na2SO4而NaClO被还原成NaCl,反应中Na2Sx与NaClO的物质的量之比为1:16,则x值是( )
分析:Na2Sx在碱性溶液中可被NaClO氧化成Na2SO4,S元素的化合价由-
价变为+6价,NaClO被还原成NaCl,Cl元素的化合价由+1价变为-1价,根据得失电子守恒计算x值.
| 2 |
| x |
解答:解:Na2Sx在碱性溶液中可被NaClO氧化成Na2SO4,S元素的化合价由-
价变为+6价,NaClO被还原成NaCl,Cl元素的化合价由+1价变为-1价,根据得失电子守恒得,
设Na2Sx的物质的量是1mol,则次氯酸钠的物质的量是16mol,
1mol×[6-(-
)]x=16mol×[1-(-1)],
1mol×[6+
]x=16mol×2
6x+2=32
x=5,
故选:D.
| 2 |
| x |
设Na2Sx的物质的量是1mol,则次氯酸钠的物质的量是16mol,
1mol×[6-(-
| 2 |
| x |
1mol×[6+
| 2 |
| x |
6x+2=32
x=5,
故选:D.
点评:本题以物质间的计算为载体考查了氧化还原反应,明确元素化合价是解本题关键,结合电子守恒解答即可,难度不大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
多硫化钠Na2Sx(x≥2)在NaOH溶液中可被NaClO氧化成Na2SO4,而NaClO被还原成NaCl,反应中Na2Sx与NaClO的物质的量之比为1:16.Na2Sx在结构上与Na2O2相似.则下列有关说法正确的是( )
| A、1mol Na2Sx参加反应,有32mol电子转移 | B、Na2Sx含有离子键和极性共价键 | C、该反应中Na2Sx是氧化剂,NaClO是还原剂 | D、Na2Sx中的x数值为2 |
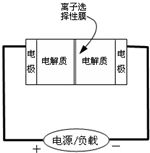 由硫可制得多硫化钠Na2Sx,x的值一般为2~6.当x=2时,多硫化钠称为过硫化钠.
由硫可制得多硫化钠Na2Sx,x的值一般为2~6.当x=2时,多硫化钠称为过硫化钠.