题目内容
如图所示,把试管放入盛有25℃时饱和石灰水的烧杯中,试管中开始放入几小块铜片,再用滴管滴入10mL稀硝酸。据此回答下列问题:
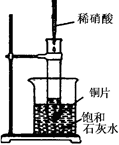
(1)实验中观察到的现象是 ;
(2)产生上述现象的原因是 ;
(3)写出有关反应的化学方程式 ;
(4)由实验推知,反应后产物的总能量 (填“大于”、“小于”、“等于”)硝酸和铜片的总能量。
(5)该装置有明显的不足,原因是 ,改进的方法是 。

(1)实验中观察到的现象是 ;
(2)产生上述现象的原因是 ;
(3)写出有关反应的化学方程式 ;
(4)由实验推知,反应后产物的总能量 (填“大于”、“小于”、“等于”)硝酸和铜片的总能量。
(5)该装置有明显的不足,原因是 ,改进的方法是 。
(1)铜片表面有气泡冒出,过一会儿,试管口附近有红棕色气体出现;烧杯中有晶体析出。
(2)铜片和稀硝酸反应生成NO,NO被氧气氧化为NO2;同时该反应放热,使烧杯内饱和石灰水的温度升高,氢氧化钙溶解度减小而析出。
(3)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,2NO+O2=2NO2
(4)小于
(5)NO、NO2逸散到空气中,会造成环境污染;在试管上加一双孔塞,用导气管将生成的气体导入到氢氧化钠溶液中。
(2)铜片和稀硝酸反应生成NO,NO被氧气氧化为NO2;同时该反应放热,使烧杯内饱和石灰水的温度升高,氢氧化钙溶解度减小而析出。
(3)3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,2NO+O2=2NO2
(4)小于
(5)NO、NO2逸散到空气中,会造成环境污染;在试管上加一双孔塞,用导气管将生成的气体导入到氢氧化钠溶液中。
铜片和稀硝酸反应有无色气体NO析出:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,故在铜片表面有气泡冒出;
NO迅速被氧气气氧化为红棕色的NO2:2NO+O2=2NO2,在试管口附近有红棕色气体出现;
由于试管内反应放热,而氢氧化钙溶解度随温度升高而减小,故烧杯饱和石灰水溶液中有晶体析出
(4)对于放热反应来讲,反应物的总能量大于生成物的总能量
(5)由于氮的氧化物均有毒,会造成空气污染,为此,可在试管上加一双孔塞,用导气管将生成的气体导入到氢氧化钠溶液中
NO迅速被氧气气氧化为红棕色的NO2:2NO+O2=2NO2,在试管口附近有红棕色气体出现;
由于试管内反应放热,而氢氧化钙溶解度随温度升高而减小,故烧杯饱和石灰水溶液中有晶体析出
(4)对于放热反应来讲,反应物的总能量大于生成物的总能量
(5)由于氮的氧化物均有毒,会造成空气污染,为此,可在试管上加一双孔塞,用导气管将生成的气体导入到氢氧化钠溶液中

练习册系列答案
 口算能手系列答案
口算能手系列答案
相关题目
 和CO;
和CO;