题目内容
【题目】由两种元素组成的矿物A,测定A的组成及制取化合物D的流程如下:
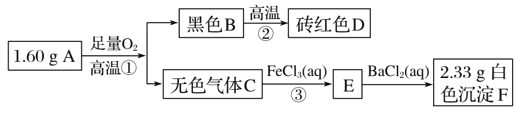
请回答:
(1)A的化学式为________________________。
(2)写出②的化学方程式:__________________。
(3)写出③的离子方程式:_________________________________________。
【答案】 Cu2S 4CuO![]() 2Cu2O+O2↑ SO2+2Fe3++2H2O=2Fe2++ SO42-+4H+
2Cu2O+O2↑ SO2+2Fe3++2H2O=2Fe2++ SO42-+4H+
【解析】试题分析:通过矿物A组成测定,考查化学方程式、离子方程式的书写,考查考生实验综合分析能力和化学计算能力。
解析:(1)砖红色物质D是Cu2O,所以黑色B为CuO,A中含有Cu元素。白色沉淀F是BaSO4,E是FeSO4,气体C是SO2,则A中含有S元素。所以A为CuS。正确答案:CuS。
(2)CuO高温分解生成Cu2O和O2,反应方程式为4CuO![]() 2Cu2O+O2↑。正确答案:4CuO
2Cu2O+O2↑。正确答案:4CuO![]() 2Cu2O+O2↑。 (3)SO2能够被Fe3+氧化生成SO42-、Fe2+,即SO2+Fe3+→SO42-+Fe2+,配平得SO2+2Fe3++2H2O=2Fe2++ SO42-+4H+。正确答案:SO2+2Fe3++2H2O=2Fe2++ SO42-+4H+。
2Cu2O+O2↑。 (3)SO2能够被Fe3+氧化生成SO42-、Fe2+,即SO2+Fe3+→SO42-+Fe2+,配平得SO2+2Fe3++2H2O=2Fe2++ SO42-+4H+。正确答案:SO2+2Fe3++2H2O=2Fe2++ SO42-+4H+。

【题目】下列离子方程式的书写及评价均合理的是( )
选项 | 离子方程式 | 评价 |
A | 将2 mol Cl2通入含1 mol FeI2的溶液中: 2Fe2++2I-+2Cl2===2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+、I-均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应: Ba2++HCO3-+OH-===BaCO3↓+H2O | 正确;酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入NaClO溶液中: SO2+H2O+ClO-===HClO+HSO3- | 正确;说明酸性:H2SO3强于HClO |
D | 1 mol/L的NaAlO2溶液和2.5 mol/L的HCl溶液等体积混合: 2AlO2-+5H+===Al3++Al(OH)3↓+H2O | 正确;第一步反应和第二步反应消耗的H+的物质的量之比为2∶3 |
A. A B. B C. C D. D