题目内容
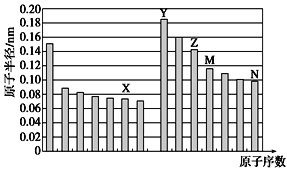
【题目】如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22。下列说法不正确的是

A.原子半径:r(X)>r(Z)>r(W)>r(Y)
B.单质Z2、Y3和Z与Y形成的化合物ZY2均可用于自来水消毒
C.X元素可形成两种或以上的单质,且在一定条件下可以相互转化
D.T元素的单质具有半导体的特性,其最高价氧化物对应水化物是一种强酸
【答案】D
【解析】
W、X、Y、Z为短周期元素,由元素在周期表中位置可知,W、Y处于第二周期,X、Z处于第三周期,假设W的最外层电子数为a,则X、Y、Z最外层电子数分别为a+1、a+2、a+3,这四种元素的原子最外层电子数之和为22,故a+a+1+a+2+a+3=22,解得a=4,则W为C、X为P、Y为O、Z为Cl、T为Ge,然后结合元素周期律及元素化合物知识来解答。
由上述分析可知,W为C、X为P、Y为O、Z为Cl、T为Ge元素。
A.由于原子核外电子层数越多、原子半径越大,同一周期的元素,从左向右原子半径减小,则原子半径:r(X)>r(Z)>r(W)>r(Y),A正确;
B.单质Z2、Y3和Z与Y形成的化合物ZY2均具有强氧化性,可用于自来水消毒,B正确;
C.X元素可形成两种或以上的单质,且在一定条件下可以相互转化,如白磷与红磷转化,C正确;
D.T元素的单质具有半导体的特性,但其最高价氧化物对应水化物是一种弱酸,酸性小于硅酸,D错误;
故合理选项是D。

 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案【题目】常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料,某探究小组利用下列反应和装置制备一硝基甲苯。


实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:①按体积比1∶3配制浓硫酸与浓硝酸混合物40mL;
②在三颈瓶中加入15mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60g。
请回答下列问题:
(1)仪器A的名称是___,使用该仪器前必须进行的操作是___。
(2)若实验后在三颈瓶中收集到的产物较少,可能的原因是___。
(3)分离反应后产物的方案如下:

其中,操作1的名称为____,操作2中需要使用下列仪器中的____(填字母)。
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(4)该实验中一硝基甲苯的产率为___(保留4位有效数字)。