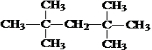题目内容
7.下列有机物在常温常压下呈气态的是( )| A. | 乙烷 | B. | 溴乙烷 | C. | 乙醇 | D. | 乙醛 |
分析 常见有机物中常温下为气态有:C原子数≤4烃、新戊烷、一氯甲烷、甲醛等,据此判断.由5到16个碳组成的烷烃常温下为液态,由17个碳以上组成的烷烃常温下为固态.
解答 解:A、乙烯中碳原子数小于4,常温下为气态,故A正确;
B、溴乙烷常温下为油状液体,故B错误;
C、乙醇常温下为无色味甜澄明黏稠液体,故C错误;
D、乙醛常温下是液态,故D错误.
故选A.
点评 本题考查了有机物的物理性质,注重了基础知识考查,注意掌握常温下为气态常见有机物,本题难度不大.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
18.下列各组中两个变化所发生的反应,属于同一反应类型的是( )
| A. | 由乙烯、氢气制取乙烷,由乙烷、溴(气体)制溴乙烷 | |
| B. | 乙烯使溴水褪色,乙炔使酸性高锰酸钾水溶液褪色 | |
| C. | 乙醇、乙酸制乙酸乙酯,由甘氨酸制得二肽 | |
| D. | 由乙烯制取聚乙烯,由甲醛、苯酚制取酚醛树脂 |
2.如表是元素周期表的短周期部分,表中字母分别表示一种元素.
请回答下列问题:
(1)g与b可形成离子化合物b2g,试写出它的电子式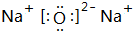 .
.
(2)e、f、g 三种元素气态氢化物的稳定性由弱到强的顺序为(用化学式表示)SiH4<NH3<H2O.
(3)在1L的密闭容器中,通入1mol f2气体和3mol a2气体,一定温度下反应生成fa3气体,2min时,测得f2的浓度为0.75mol•L-1,则2min时fa3的物质的量为0.5mol,a2的化学反应速率v(a2)=0.375 mol•(L•min)-1.
(4)a、d两种元素可形成多种化合物,其中化合物X是最简单的有机物,已知常温下4g X在O2中完全燃烧放出222.4KJ的热量,试写出化合物X完全燃烧的热化学方程式:CH4(g)+2O2(g)→CO2(g)+2H2O(1)H=-889.6kJ/mol.
(5)航天技术中常使用a和g单质组成的碱性燃料电池,该电池具有高能、轻便和不污染环境等优点.该电池正极电极反应式为O2+2H2O+4e-=4OH-.
| a | |||||||
| d | f | g | |||||
| b | c | e | h | ||||
(1)g与b可形成离子化合物b2g,试写出它的电子式
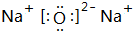 .
.(2)e、f、g 三种元素气态氢化物的稳定性由弱到强的顺序为(用化学式表示)SiH4<NH3<H2O.
(3)在1L的密闭容器中,通入1mol f2气体和3mol a2气体,一定温度下反应生成fa3气体,2min时,测得f2的浓度为0.75mol•L-1,则2min时fa3的物质的量为0.5mol,a2的化学反应速率v(a2)=0.375 mol•(L•min)-1.
(4)a、d两种元素可形成多种化合物,其中化合物X是最简单的有机物,已知常温下4g X在O2中完全燃烧放出222.4KJ的热量,试写出化合物X完全燃烧的热化学方程式:CH4(g)+2O2(g)→CO2(g)+2H2O(1)H=-889.6kJ/mol.
(5)航天技术中常使用a和g单质组成的碱性燃料电池,该电池具有高能、轻便和不污染环境等优点.该电池正极电极反应式为O2+2H2O+4e-=4OH-.
12.下列有机物在水中的溶解度,排序正确的是( )
a.HOCH2CH2CH2OH b.CH3CH2CH2OH
c.CH3CH2COOCH3 d.
a.HOCH2CH2CH2OH b.CH3CH2CH2OH
c.CH3CH2COOCH3 d.

| A. | d>b>c>a | B. | c>d>a>b | C. | d>a>b>c | D. | c>d>b>a |
19.下列物质中,属于顺式结构的是( )
| A. | 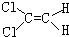 | B. | 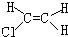 | C. | 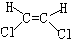 | D. | 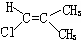 |
2.据报道,有一种叫Thibacillus Ferroxidans的细菌在氧气存在下的酸性溶液中,能将黄铜矿(CuFeS2)氧化成硫酸盐.发生的反应为:4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
(1)CuFeS2中Fe的化合价为+2,上述反应中被氧化的元素是Fe和CuFeS2中的S.
(2)工业生产中利用上述反应后的溶液,按如图甲流程可制备胆矾(CuSO4•5H2O):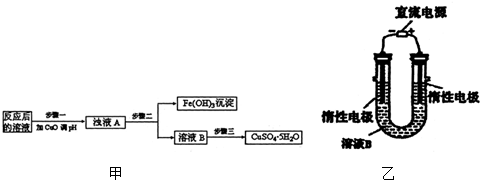
①分析表格(其中KSP是相应金属氢氧化物的沉淀溶解平衡常数):
步骤一应调节溶液的pH范围是3.2≤pH<4.7.请运用沉淀溶解平衡的有关理论解释加入CuO能除去CuSO4溶液中Fe3+的原因加入CuO与H+反应使c(H+)减小,c(OH-)增大,使溶液中c(Fe3+)•c3(OH-)>Ksp[Fe(OH)3],导致Fe3+生成沉淀而除去.
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶.
(3)有人提出可以利用图乙的装置从溶液B中提炼金属铜.该过程中图乙电极的反应式是4OH--4e-=O2↑+2H2O,总反应的方程式是2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+2H2SO4+O2↑.
(1)CuFeS2中Fe的化合价为+2,上述反应中被氧化的元素是Fe和CuFeS2中的S.
(2)工业生产中利用上述反应后的溶液,按如图甲流程可制备胆矾(CuSO4•5H2O):

①分析表格(其中KSP是相应金属氢氧化物的沉淀溶解平衡常数):
| Ksp | 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.6×10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2×10-20 | 4.7 | 6.7 |
②步骤三中的具体操作方法是蒸发浓缩,冷却结晶.
(3)有人提出可以利用图乙的装置从溶液B中提炼金属铜.该过程中图乙电极的反应式是4OH--4e-=O2↑+2H2O,总反应的方程式是2CuSO4+2H2O$\frac{\underline{\;电解\;}}{\;}$2Cu+2H2SO4+O2↑.
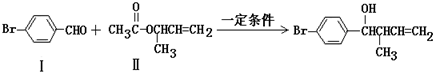

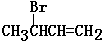 .
.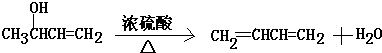 (注明反应条件).在碱性条件下,由Ⅳ与
(注明反应条件).在碱性条件下,由Ⅳ与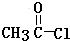 反应合成Ⅱ,其反应类型为取代反应.
反应合成Ⅱ,其反应类型为取代反应.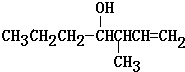 (写出其中一种).
(写出其中一种).