题目内容
【题目】将氢氧化钠稀溶液滴加到醋酸稀溶液中,下列各图表示混合溶液有关量或性质的变化趋势,其中错误的是

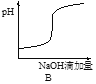
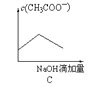
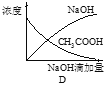
A. A B. B C. C D. D
【答案】D
【解析】A.氢氧化钠和醋酸发生中和反应,反应放热,当酸反应完成后,再加碱,相当于往热水中加入冷水,温度降低,故A正确;B.醋酸中滴加氢氧化钠酸性减弱pH增大,当酸碱恰好发生中和时,pH突变,醋酸完全反应后,溶液碱性逐渐增强,故B正确;C.醋酸中滴加氢氧化钠,生成强电解质CH3COONa,溶液中CH3COO-浓度逐渐增大,当完全反应后,继续滴加NaOH溶液,溶液体积增大,CH3COO-浓度逐渐减小,因此导电能力增加,故C正确;D.醋酸中滴加氢氧化钠,氢氧化钠和醋酸发生反应了,当醋酸剩余时,氢氧化钠物质的量0,醋酸中滴加氢氧化钠,即便醋酸完全反应,醋酸钠还是有微弱的水解,醋酸的浓度不可能为0,故D错误;故答案为D。

练习册系列答案
相关题目