题目内容
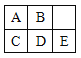
【题目】下图是元素周期表的一部分,表中所列字母a、b、c、d、e、f、g、h分别代表某种化学元素。请依据这8种元素回答下列问题。

(1)上述8种元素的单质中常温下为气态,且密度最小的是______(填化学式)。
(2)f元素的原子结构示意图为_______。
(3)c的最高价氧化物对应水化物的化学式为______。
(4)hg的电子式为_______。
(5)b、c、d三种元素的最简单氢化物的沸点由高到低的顺序是______(填化学式)。
(6)元素e的单质与h的最高价氧化物对应的水化物反应的化学方程式为__________。
(7)f元素的最简单氢化物的水溶液显____性(填“酸”或“碱”),请写出该氢化物久置在空气中变质的化学方程式________。
(8)gd-常用作消毒剂,单质砷(As)在碱性溶液中可被gd-氧化为AsO43-,该反应的离子方程式为__________。
【答案】 H2  HNO3
HNO3 ![]() H2O>NH3>CH4 2Al+2KOH+2H2O=2KAlO2+3H2↑ 酸 2H2S+O2=2S↓+2H2O 5ClO-+2As+6OH-=2AsO43-+5Cl-+3H2O
H2O>NH3>CH4 2Al+2KOH+2H2O=2KAlO2+3H2↑ 酸 2H2S+O2=2S↓+2H2O 5ClO-+2As+6OH-=2AsO43-+5Cl-+3H2O
【解析】根据元素周期表的结构以及各元素在周期表中的位置,a、b、c、d、e、f、g、h分别代表H、C、N、O、Al、S、Cl、K元素。用元素周期律和相关化学用语作答。
根据元素周期表的结构以及各元素在周期表中的位置,a、b、c、d、e、f、g、h分别代表H、C、N、O、Al、S、Cl、K元素。
(1)上述8种元素的单质中常温下为气态,且密度最小的是H2。
(2)f为S元素,S的核电荷数为16,S原子核外有16个电子,根据原子核外电子排布规律,S的原子结构示意图为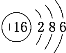 。
。
(3)c为N元素,N原子最外层有5个电子,N元素的最高化合价为+5价,N的最高价氧化物为N2O5,N的最高价氧化物对应水化物的化学式为HNO3。
(4)hg为KCl,KCl中只含离子键,KCl的电子式为![]() 。
。
(5)b、c、d三种元素的最简单氢化物依次为CH4、NH3、H2O,CH4分子间不存在氢键,NH3分子间、H2O分子间存在氢键,且H2O分子间氢键强于NH3分子间氢键,b、c、d三种元素的最简单氢化物的沸点由高到低的顺序为H2O![]() NH3
NH3![]() CH4。
CH4。
(6)元素e的单质为Al,h为K元素,h的最高价氧化物对应的水化物为KOH,Al与KOH溶液反应的化学方程式为2Al+2KOH+2H2O=2KAlO2+3H2↑。
(7)f为S元素,S原子的最外层有6个电子,S的最低负价为-2价,f元素的最简单氢化物为H2S,H2S的水溶液为氢硫酸,氢硫酸显酸性。H2S在空气中久置被空气中氧气氧化成S,反应的化学方程式为O2+2H2S=2S↓+2H2O。
(8)gd-为ClO-,As在碱性溶液中可被ClO-氧化成AsO43-,则ClO-被还原成Cl-,反应可写成As+ClO-→AsO43-+Cl-,在反应中As元素的化合价由0价升至+5价,Cl元素的化合价由+1价降至-1价,根据得失电子守恒可配平为2As+5ClO-→2AsO43-+5Cl-,结合碱性溶液、原子守恒和电荷守恒,反应的离子方程式为2As+5ClO-+6OH-=2AsO43-+5Cl-+3H2O。

 全优点练单元计划系列答案
全优点练单元计划系列答案