题目内容
14.请完成下列填空,每空2分.(1)标准状况下,11.2LCO2的物质的量0.5 mol,质量22g,含NA或6.02×1023个氧原子.(已知:CO2 相对分子质量为44)
(2)某BaCl2溶液100mL,其中含1.204×1023个Cl-,求n(BaCl2)=0.1mol,溶液中c(Ba2+)=1mol/L
(3)某学生欲用12mol•L-1浓盐酸和蒸馏水配制500mL物质的量浓度为0.60mol/L的稀盐酸.该学生需要量取25 mL上述浓盐酸进行配制.
(4)在 200mL 0.5mol/L H2SO4 溶液中,c(H+)=1mol/L,溶质的质量是9.8g.此溶液中含 n(H+)=0.2mol (已知H2SO4 相对分子质量为98)
分析 (1)(2)根据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$结合分子的构成计算;
(3)(4)根据n=cV=$\frac{m}{M}$计算.
解答 解:(1)n(CO2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,m(CO2)=0.5mol×44g/mol=22g,n(O)=1mol,N(O)=NA 或6.02×1023;
故答案为:0.5; 22;NA 或6.02×1023;
(2)n(Cl-)=$\frac{1.204×1{0}^{23}}{6.02×1{0}^{23}/mol}$=0.2mol,n(BaCl2)=$\frac{1}{2}$n(Cl-)=0.1mol,c(Ba2+)=$\frac{0.1mol}{0.1L}$=1mol/L,
故答案为:0.1 mol;1mol/L;
(3)500mL物质的量浓度为0.60mol/L的稀盐酸中n(HCl)=0.5L×0.60mol/L=0.3mol,
V=$\frac{0.3mol}{12mol/L}$=0.025L=25mL,
故答案为:25;
(4)n(H2SO4)=0.2L×0.5mol/L=0.1mol,n(H+)=0.2mol,c(H+)=$\frac{0.2mol}{0.2L}$=1mol/L,m(H2SO4)=0.1mol×98g/mol=9.8g,n(H+)=2n(H2SO4)=0.2mol,
故答案为:1mol/L; 9.8 g; 0.2mol.
点评 本题综合考查物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用以及物质的构成,难度不大.

练习册系列答案
相关题目
5.化学家们合成了如图所示的一系列的星烷,如三星烷、四星烷、五星烷等.下列说正确的( )


| A. | 六星烷的化学式为C18H24 | |
| B. | 它们之间互为同系物 | |
| C. | 三星烷与丙苯互为同分异构体,四星烷与 互为同分异构体 互为同分异构体 | |
| D. | 星烷的一氯代物均只有2种,而三星烷的二氯代物有4种 |
2.下列各物质的分类、名称(或俗名)、化学式都正确的是( )
| A. | 金属氧化物 过氧化钠 Na2O | B. | 酸 硫酸 H2SO4 | ||
| C. | 盐 苛性钠 NaOH | D. | 碱 纯碱 Na2CO3 |
9.下列操作中发生复分解反应的是( )
| A. | 将碳酸钾加入氯化钠溶液中 | B. | 在硫酸铜溶液中加入铁片 | ||
| C. | 在盐酸中加入氢氧化钠溶液 | D. | 让铁丝在氧气中燃烧 |
6.想一想:Ba(OH)2(固态)、CuSO4(固态)、CH3COOH(液态)这些物质为什么归为一类,下列哪个物质还可以和它们归为一类( )
| A. | 75%的酒精溶液 | B. | 硝酸钠(固态) | C. | Fe(OH)3胶体 | D. | 豆浆 |
3.利用如图所示的有机物X可生产S-诱抗素Y.下列说法正确的是( )


| A. | 1mol X与足量NaOH溶液反应,最多消耗4mol NaOH | |
| B. | Y既可以与FeCl3溶液发生显色反应,又可使酸性KMnO4溶液褪色 | |
| C. | X可以发生氧化、取代、酯化、加聚、缩聚反应,并能与盐酸反应生成有机盐 | |
| D. | X结构中有2个手性碳原子 |
4. 在密闭容器中存在反应:2SO2(g)+O2(g)═2SO3(g)△H<0,某研究小组研究该反应后作出了如图所示曲线.下列分析正确的是( )
在密闭容器中存在反应:2SO2(g)+O2(g)═2SO3(g)△H<0,某研究小组研究该反应后作出了如图所示曲线.下列分析正确的是( )
 在密闭容器中存在反应:2SO2(g)+O2(g)═2SO3(g)△H<0,某研究小组研究该反应后作出了如图所示曲线.下列分析正确的是( )
在密闭容器中存在反应:2SO2(g)+O2(g)═2SO3(g)△H<0,某研究小组研究该反应后作出了如图所示曲线.下列分析正确的是( )| 选项 | Y的物理意义 | 甲、乙的物理意义 | 甲与乙的大小 |
| A | SO2的转率 | 温度 | 甲>乙 |
| B | SO2的体积分数 | 压强 | 甲>乙 |
| C | SO3的体积分数 | 温度 | 乙>甲 |
| D | SO2的转率 | 压强 | 乙>甲 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
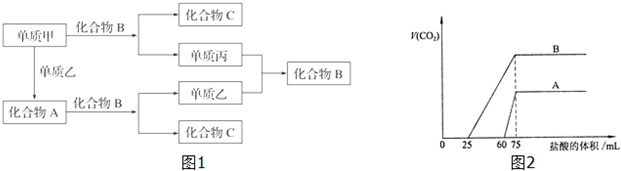
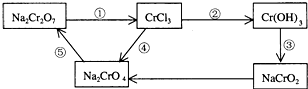 化学实验中,如果使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质.
化学实验中,如果使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质.