题目内容
4.下列离子方程式书写不正确的是( )| A. | 铝粉投入到NaOH溶液中:2Al+2OH-+2 H2O→2AlO2-+3H2↑ | |
| B. | Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-→2AlO2-+H2O | |
| C. | 铁跟稀硫酸反应:2Fe+6H+→2Fe3++3H2↑ | |
| D. | 氧化亚铁放入盐酸中:FeO+2H+→Fe2++H2O |
分析 A.二者反应生成偏铝酸钠和氢气;
B.二者反应生成偏铝酸钠和水;
C.不符合反应客观事实;
D.二者反应生成氯化亚铁和水.
解答 解:A.铝粉投入到NaOH溶液中,离子方程式:2Al+2OH-+2 H2O→2AlO2-+3H2↑,故A正确;
B.Al2O3粉末溶于NaOH溶液中,离子方程式:Al2O3+2OH-→2AlO2-+H2O,故B正确;
C.铁跟稀硫酸反应生成硫酸亚铁和氢气,离子方程式:Fe+2H+=Fe2++H2↑,故C错误;
D.氧化亚铁放入盐酸中,离子方程式:FeO+2H+=Fe2++H2O,故D正确;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意离子反应必须遵循客观事实.

练习册系列答案
相关题目
16. 如图所示为某原电池的结构示意图,下列说法不正确的是(盐桥中装满用饱和KCl溶液和琼胶做成的冻胶)( )
如图所示为某原电池的结构示意图,下列说法不正确的是(盐桥中装满用饱和KCl溶液和琼胶做成的冻胶)( )
 如图所示为某原电池的结构示意图,下列说法不正确的是(盐桥中装满用饱和KCl溶液和琼胶做成的冻胶)( )
如图所示为某原电池的结构示意图,下列说法不正确的是(盐桥中装满用饱和KCl溶液和琼胶做成的冻胶)( )| A. | 该原电池的总反应式为2Fe3++Cu=2Fe2++Cu2+ | |
| B. | 电池工作过程中,电子由铜电极经过电流表流向石墨电极 | |
| C. | 该电池工作时,Cu2+在电极上得到电子,发生还原反应 | |
| D. | 若用此电池电解饱和氯化钠溶液制取Cl2,当铜电极的质量减少6.4 g时,产生标准状况下氯气的体积为2.24 L |
19.下列各元素中,化合价的最高正价数最大的是( )
| A. | F | B. | S | C. | N | D. | Al |
9.下列说法正确合理的是( )
| A. | 随着化学科学的发展,已发现了大量新分子,但还没有合成出自然界不存在的新分子 | |
| B. | 凡是纯天然的物质,一定比人工制造、合成的物质好 | |
| C. | “碘盐”、“增铁酱油”、“高钙牛奶”等商品.这里的碘、铁、钙指的是元素 | |
| D. | 从自然界中获得物质,都是化合态的物质 |

 爆鸣声和火花;然后过滤、洗涤、干燥;最后称量、计算,测得其产率只有预期值的63%左右。
爆鸣声和火花;然后过滤、洗涤、干燥;最后称量、计算,测得其产率只有预期值的63%左右。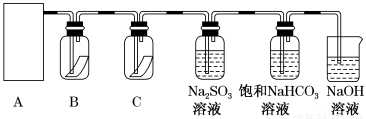
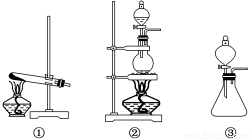
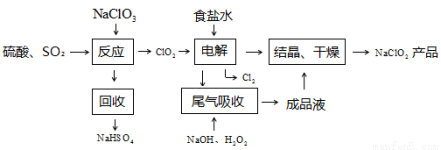
 化合价为 。
化合价为 。