题目内容
如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )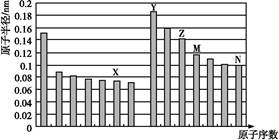
| A.N、Z两种元素的离子半径相比前者较大 |
| B.M、N两种元素的气态氢化物的稳定性相比后者较强 |
| C.X与M两种元素组成的化合物能与碱反应,但不能与任何酸反应 |
| D.工业上常用电解Y和N形成的化合物的熔融态制取Y的单质 |
C
解析

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
下列判断错误的是( )
| A.沸点:NH3>PH3>AsH3 |
| B.熔点:Si3N4>NaCl>SiI4 |
| C.酸性:HClO4>H2SO4>H3PO4 |
| D.碱性:NaOH>Mg(OH)2>Al(OH)3 |
X、Y、Z、R、W是5种短周期元素,原子序数依次增大;它们可组成离子化合物Z2Y和共价化合物RY3、XW4;已知Y、R同主族,Z、R、W同周期。下列说法错误的是( )
| A.Y、Z、R 3种元素组成的化合物水溶液一定显碱性 |
| B.原子半径:Z>R>W |
| C.气态氢化物稳定性:HW>H2R |
| D.XW4分子中各原子均满足8电子结构 |
X、Y、Z、R、W是原子序数依次增大的五种短周期元素。Y和R同主族,可组成共价化合物RY2,Y和Z最外层电子数之和与W的最外层电子数相同,25 ℃时,0.1 mol/L X和W形成化合物的水溶液pH为1。下列说法正确的是( )
| A.由于相对原子质量R>Y,所以X、R组成化合物的沸点高于X、Y组成的化合物 |
| B.Y和其他四种元素均可形成至少两种二元化合物 |
| C.RY2能与Y、Z形成的一种化合物反应生成Y2 |
| D.Y、Z、W三种元素组成化合物的水溶液一定显碱性 |
依据元素周期表及元素周期律,下列推断正确的是( )
| A.H3BO3的酸性比H2CO3的强 |
| B.Mg(OH)2的碱性比Be(OH)2的强 |
| C.HCl、HBr、HI的热稳定性依次增强 |
| D.若M+和R2-的核外电子层结构相同,则原子序数:R>M |
元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是( )
| A.所有元素原子的最外层电子数都等于元素的最高化合价 |
| B.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强 |
| C.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 |
短周期元素T、X、Y、Z的原子序数依次增大,T与Z属于同一主族,X、Y、Z最高价氧化物对应的水化物两两之间都能反应,且X、Y、Z原子最外层电子数之和等于X的原子序数。则下列说法正确的是( )。
| A.简单离子半径大小顺序:r(T)>r(X)>r(Y) |
| B.T与Z的最高正化合价相等 |
| C.室温下,单质Y不能与浓硫酸反应 |
| D.用电解法可制得T、X、Y的单质 |