��Ŀ����
����Ŀ��ij��Һ�п��ܺ���H+��Fe2+��Mg2+��Cu2+��NH4+��A13+��OH-��SO42- �е�һ�ֻ��֡�������һ�ֵ���ɫ���岢������Һʱ���д̼�����ζ������ų��Ͱ�ɫ�������������뵭��ɫ��������ʵ���(������)�����������Ͳ�����������ʵ���(������)�Ĺ�ϵ����ͼ��ʾ������д���пհ�:
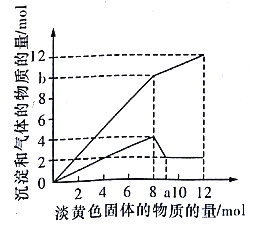
��1��ͼ��a���ֵ��__________�����ӵĵ���ɫ������_________ (�ѧʽ)��
��2������Һ�к��е�������_________��
��3����μ�����Һ�д��ڵ�������? _________��
���𰸡� 9 Na2O2 Mg2+��Al3+��NH4+��SO42- �ȼ�ϡ�������������������ټ��Ȼ�����Һ���а�ɫ��������
������������ɫ���������Һ�У���������Һʱ���д̼�������ų��Ͱ�ɫ�������ɣ���ɫ����ΪNa2O2��ͼ��ʵ��Ϊ����ͼ����һ�𣬽��ϵ������壬���µ��dz�����ͼ���м���8mol�������ƺ�ɫ������С����û����ȫ�ܽ⣬����Һ��һ��û��Fe2+��Cu2+��һ����NH4+��Al3+��Mg2+����Һ�б�����������ӣ�ֻ����SO42-������8mol��������֮�����������С��˵������8mol��������ʱ��笠�������ȫ��Ӧ��ֻ�ų�������
(1)���������֪��n(Mg2+)=n[Mg(OH)2]=2mol��n(Al3+)=4mol-n[Mg(OH)2]=2mol����2mol���������ܽ�ֻ��Ҫ2mol�������ƣ���1mol�������ƣ����a=9��������������֪������ɫ����Ϊ��Na2O2���ʴ�Ϊ��9��Na2O2��
(2)����������������Һ�к��е�������Mg2+��Al3+��NH4+��SO42-���ʴ�Ϊ��Mg2+��Al3+��NH4+��SO42-��
(3)������������ӿ�������Һ���ȼ�ϡ���ᣬ�����������ټ��Ȼ�����Һ���а�ɫ�����������ʴ�Ϊ���ȼ�ϡ���ᣬ�����������ټ��Ȼ�����Һ���а�ɫ����������

����Ŀ�����ĵ��ʼ��仯�������ʶ�������;�㷺�� ���������գ�
��1����ѧ�������о����ô������������ٷɻ�β���е�NO��COת���CO2��N2��2NO+2CO ![]() 2CO2+N2+Q��Q��0�� ij�¶��²�ø÷�Ӧ�ڲ�ͬʱ���COŨ�������
2CO2+N2+Q��Q��0�� ij�¶��²�ø÷�Ӧ�ڲ�ͬʱ���COŨ�������
ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
c��CO�� | 3.60��10��3 | 3.05��10��3 | 2.85��10��3 | 2.75��10��3 | 2.70��10��3 | 2.70��10��3 |
�÷�Ӧƽ�ⳣ��K�ı���ʽΪ���¶����ߣ�Kֵ��ѡ���������С���������䡱����ǰ2s�ڵ�ƽ����Ӧ����v��N2��=����������Ӧ���ܱ������з������ﵽƽ��ʱ�����NOת���ʵĴ�ʩ֮һ�� ��
��2����ҵ�ϳɰ��ķ�Ӧ�¶�ѡ��500�����ҵ�ԭ���� ��
��3��ʵ�����ڹ̶��ݻ����ܱ������м���1mol������3mol����ģ�ҵ�ϳɰ�����Ӧ��һ���������Ѵﵽƽ��ı�־�� �� a��N2��H2��NH3��Ũ��֮��Ϊ1��3��2
b�������ڵ�ѹǿ���ֲ���
c��N2��H2��NH3��Ũ�Ȳ��ٷ����仯
d����Ӧֹͣ�������淴Ӧ�����ʶ�������
��4����������1mol���ʵ�ϡ�����л���ͨ��1mol NH3����Һ����仯���Բ��ƣ�����Ӧ��������Һ������Ũ���ɴ�С��˳��������ͨ��NH3�Ĺ�������Һ�ĵ���������ѡ��������С�������������䡱����