题目内容
【题目】电解原理在化学工业中有着广泛的应用。下图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
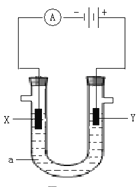
(1)若用U型管电解滴有酚酞的饱和食盐水,电解一段时间后,_________极(选填X或Y)附近溶液呈红色, Y极产生的现象是______________________,电解前溶液的pH_______7(填“大于”、“小于”或“等于”,下同),电解后溶液的pH_________7。
(2)写出电解饱和食盐水的化学方程式____________________________________________ 。
(3)若a是CuCl2溶液,则Y极上的产物是____________。X极现象____________________________。
【答案】X 产生黄绿色气体 等于 大于 2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑ Cl2 析出紫红色金属
2NaOH+H2↑+Cl2↑ Cl2 析出紫红色金属
【解析】
(1)X电极上氢离子放电生成氢气,同时电极附近生成氢氧根离子,导致溶液呈碱性,酚酞遇碱变红色;Y电极上氯离子放电生成氯气;
(2)惰性电极电解饱和食盐水生成NaOH、氯气和氢气;
(3)若a是CuCl2溶液,Cu2+在X极上得电子发生还原反应,Cl-在Y极上发生氧化反应。
(1)和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红;Y极为阳极,溶液中Cl-在Y极上发生氧化反应生成氯气,现象是产生黄绿色气体,电解前NaCl溶液呈中性,溶液的pH等于7,电解后生成NaOH,溶液的pH大于7;
(2)惰性电极电解饱和食盐水生成NaOH、氯气和氢气,发生反应的化学方程式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
(3)若a是CuCl2溶液,Cu2+在X极上得电子发生还原反应,Cl-在Y极上发生氧化反应,则Y极上的产物是Cl2;X极看到的现象是析出紫红色金属。

 名校课堂系列答案
名校课堂系列答案【题目】一定温度下,在1L恒容密闭容器中加入lmol的N2(g)和3molH2(g)发生反应:N2(g)+3H2(g) ![]() 2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法不正确的是( )
2NH3(g) △H<0, NH3的物质的量与时间的关系如下表所示,下列说法不正确的是( )
时间(min) | 0 | t1 | t2 | t3 |
NH3物质的量(mol) | 0 | 0.2 | 0.3 | 0.3 |
A. 0t1min,v(NH3)=0.2/t1mol·L-1·min-1
B. t3时再加入1mol的N2(g)和3molH2(g),反应达新平衡时,c(N2)>0.85mol·L-1
C. N2(g)+3H2(g) ![]() 2NH3(g)的活化能小于2NH3(g)
2NH3(g)的活化能小于2NH3(g) ![]() N2(g)+3H2(g)的活化能
N2(g)+3H2(g)的活化能
D. 升高温度,可使正反应速率减小,逆反应速率增大,故平衡逆移