题目内容
【题目】如图1是某化学兴趣小组进行丁烷裂解的实验流程.(注:CuO能将烃氧化成CO2和H2O,G后面装置与答题无关,铁架台等已省略.)按下图连好装置后,需进行的实验操作有:①给D、G装置加热;②检查整套装置的气密性;③排出装置中的空气等…
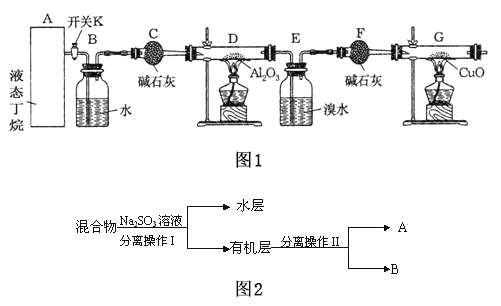
(1)这三步操作的先后顺序依次是_________________;
(2)B装置所起的作用是________________;
(3)假定丁烷按C4H10→C2H6+C2H4和C4H10→CH4+C3H6的方式完全裂解,当(E+F)装置的总质量比反应前增加了0.7g,G装置的质量减少了1.76g,则丁烷的裂解产物中,甲烷与乙烷的物质的量之比为 ____________________(假定流经D、G装置中的气体能完全反应)。
(4)若对E装置中的混合物再按图2流程实验:
①分离操作Ⅰ和Ⅱ的名称分别是:Ⅰ ______________,分液Ⅱ_____________;
Na2SO3溶液的作用是____________(用离子方程式表示)。
②已知B的碳原子数大于A的碳原子数,请写出B的结构简式___________。
【答案】 ②③① 通过观察气泡,调节K,控制气体流速 1:1 分液 蒸馏 SO32-+Br2+H2O═SO42-+2H++2Br- CH3-CHBr-CH2Br
【解析】本题考查实验操作,实验计算,离子方程式的书写,物质分离和提纯的方法,难度较大.
(1)装置连接好以后。首先检验装置的气密性,所以顺序是②③①;(2)B中是水,所以可以通过观察气泡,可以通过调节开关K控制气体的流速,从而控制丁烷气体的流量;(3)设甲烷和乙烷的物质的量分别是x、y,则根据方程式可知丙烯和乙烯也分别是x、y。 “当(E+F)装置的总质量比反应前增加了0.7g”,根据质量守恒可以知道烯烃的质量为0.7g,则有28x+42y=0.7g;G装置的质量减少了1.76,根据CuO能将烃氧化成CO2和H2O,可知氧化铜减少的质量是氧原子的质量,即和烷烃结合的氧原子是0.11mol,再根据氧原子的守恒则有:2(2x+y)+ ![]() =0.11mol,解得:x=y=0.01mol。甲烷与乙烷的物质的量之比为1:1;(4)①分离操作I是加入亚硫酸钠后分离后得到水层和有机层,因亚硫酸钠与有机物不互溶,故分离不互溶的液体用分夜;分离操作II是分离有机层得到有机物A和B,故分离互溶的液体用蒸馏; Na2SO3溶液可吸收溴单质;②由B的碳原子数大于A的碳原子数可知B为二溴丙烷CH3-CHBr-CH2Br,A为二溴乙烷CH2Br-CH2Br。
=0.11mol,解得:x=y=0.01mol。甲烷与乙烷的物质的量之比为1:1;(4)①分离操作I是加入亚硫酸钠后分离后得到水层和有机层,因亚硫酸钠与有机物不互溶,故分离不互溶的液体用分夜;分离操作II是分离有机层得到有机物A和B,故分离互溶的液体用蒸馏; Na2SO3溶液可吸收溴单质;②由B的碳原子数大于A的碳原子数可知B为二溴丙烷CH3-CHBr-CH2Br,A为二溴乙烷CH2Br-CH2Br。