题目内容
如图是某条件时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是


A.该反应的热化学方程式为:2NH3  N2+3H2ΔH =-92 kJ·mol-1 N2+3H2ΔH =-92 kJ·mol-1 |
| B.正反应的活化能小于逆反应的活化能 |
| C.a曲线是加入催化剂时的能量变化曲线 |
| D.加入催化剂可增大正反应速率,降低逆反应速率 |
B
试题分析:由图像可知A项的热化学方程式应为2NH3(g)
 N2(g)+3H2(g) ΔH ="+92" kJ·mol-1,错误;B项正确;C项b曲线表示加入了催化剂;D项加入催化剂正逆反应速率均增大,错误。
N2(g)+3H2(g) ΔH ="+92" kJ·mol-1,错误;B项正确;C项b曲线表示加入了催化剂;D项加入催化剂正逆反应速率均增大,错误。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 2SO3(g),混合体系中SO3的百分含量和温度的关系如下图1所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
2SO3(g),混合体系中SO3的百分含量和温度的关系如下图1所示(曲线上任何一点都表示平衡状态).根据图示回答下列问题:
 2AB3(g)化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
2AB3(g)化学平衡状态的影响,得到如下图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是
 >
> ,则正反应一定是放热反应
,则正反应一定是放热反应 的转化率大小为:b>a>c
的转化率大小为:b>a>c >
>
 不变时达到平衡,
不变时达到平衡,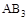 的物质的量大小为:c>b>a
的物质的量大小为:c>b>a