题目内容
【题目】下列关于纯净物、混合物、电解质、非电解质的正确组合是( )
纯净物 | 混合物 | 电解质 | 非电解质 | |
A | 盐酸 | 冰水混合物 | 硫酸 | 干冰 |
B | 蒸馏水 | 蔗糖溶液 | 氧化铝 | 二氧化硫 |
C | 明矾 | 盐酸 | 铁 | 碳酸钙 |
D | 胆矾 | 食盐水 | 氯化铜 | 碳酸钠 |
【答案】B
【解析】
试题分析:A. 盐酸是HCl的水溶液,属于混合物,不是纯净物,错误;B.各种物质分类标准正确;C.Fe是金属单质,不是化合物,因此不属于电解质,错误;D. 碳酸钠是盐,属于电解质,错误。

 出彩同步大试卷系列答案
出彩同步大试卷系列答案【题目】目前人们对环境保护、新能源开发很重视.
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体.4CO(g)+2NO2(g)4CO2(g)+N2(g)△H=﹣1200 kJmol﹣1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图象正确的是(填代号). 
(2)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g)N2(g)+CO2(g)△H在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
浓度/mol.L﹣1/时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①根据图表数据分析T1℃时,该反应在0~20min的平均反应速率v(CO2)=;计算该反应的平衡常数K= .
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是(填字母代号).
a.加入一定量的活性炭 b.通入一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率(填“升高”或“降低”),△H0(填“>”或“<”).
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2].已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s)△H=﹣159.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g)△H=+116.5kJ/mol
③H2O(l)=H2O(g)△H=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式 .
(4)一种氨燃料电池,使用的电解质溶液是2mol/L﹣1的KOH溶液.
电池反应为:4NH3+3O2=2N2+6H2O;
请写出通入a气体一极的电极反应式为;每消耗3.4g NH3转移电子的物质的量为 .
【题目】苯甲酸甲酯是一种重要的工业原料,某研究性学习小组的同学拟用如图装置制取高纯度的苯甲酸甲酯. 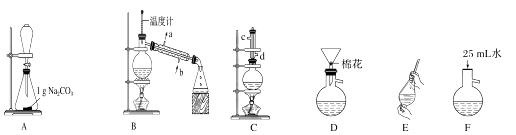
熔点/℃ | 沸点/℃ | 密度/gcm﹣3 | 水溶性 | |
苯甲酸 | 122.4 | 249 | 1.27 | 微溶 |
甲醇 | ﹣97 | 64.3 | 0.79 | 互溶 |
苯甲酸甲酯 | ﹣12.3 | 199.6 | 1.09 | 不溶 |
有关数据如表所示,请回答下列问题:
(1)在烧瓶中混合有机物及浓硫酸的方法是 , 装置C如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是 .
(2)B装置的冷凝管的主要作用是 , 可否换为球形冷凝管(填“可”或“否”).
(3)制备和提纯苯甲酸甲酯的操作先后顺序为(填装置字母代号).
(4)A中Na2CO3的作用是;D装置的作用是
(5)在洗涤、分液操作中,应充分振荡,然后静置,待分层后(填标号). a.直接将苯甲酸甲酯从分液漏斗的上口倒出
b.直接将苯甲酸甲酯从分液漏斗的下口放出
c.先将水层从分液漏斗的下口放出,再将苯甲酸甲酯从下口放出
d.先将水层从分液漏斗的下口放出,再将苯甲酸甲酯从上口倒出.