题目内容
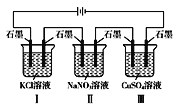
【题目】如图装置电解一段时间,当某极析出0.32 g Cu时,Ⅰ、Ⅱ、Ⅲ中溶液pH分别为(常温下,溶液足量,体积均为100 mL且电解前后溶液的体积变化忽略不计)( )
A. 12、7、2 B. 13、7、1 C. 1、7、13 D. 7、13、1
【答案】B
【解析】n(Cu)= ![]() =0.005mol,由电极反应Cu2++2e-=Cu可知转移电子为0.01mol,电解时,I、Ⅱ、Ⅲ中溶液电池反应方程式分别为2KCl+2H2O
=0.005mol,由电极反应Cu2++2e-=Cu可知转移电子为0.01mol,电解时,I、Ⅱ、Ⅲ中溶液电池反应方程式分别为2KCl+2H2O![]() 2KOH+H2↑+Cl2↑、2H2O
2KOH+H2↑+Cl2↑、2H2O![]() 2H2↑+O2↑、2CuSO4+2H2O
2H2↑+O2↑、2CuSO4+2H2O![]() 2Cu+O2↑+2H2SO4,I中生成0.01molOH-,c(OH-)=
2Cu+O2↑+2H2SO4,I中生成0.01molOH-,c(OH-)=![]() =0.1mol/L,pH=13,Ⅱ电解水,溶液呈中性,pH=7,Ⅲ中生成0.01molH+,c(H+)=
=0.1mol/L,pH=13,Ⅱ电解水,溶液呈中性,pH=7,Ⅲ中生成0.01molH+,c(H+)=![]() =0.1mol/L,pH=1,故选B。
=0.1mol/L,pH=1,故选B。

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目