题目内容
(15分)工业上制取铝的流程如下:
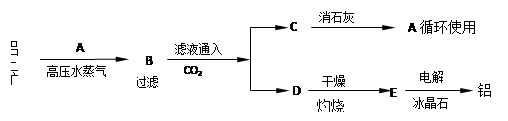
注:冰晶石的作用是使E在较低温度下熔化。
(1)试写出下列物质的化学式:
A ,B ,C ,D ,E 。
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
试求制取1t Al2O3所需铝土矿和苛性钠的质量。(写过程)

注:冰晶石的作用是使E在较低温度下熔化。
(1)试写出下列物质的化学式:
A ,B ,C ,D ,E 。
(2)在用此法制取铝时,分析铝土矿和赤泥(提取Al2O3之后的残渣)所得数据如下:
| | Al2O3 | Fe2O3 | Na2O |
| 铝土矿 | 55% | 16% | 0% |
| 赤泥 | 15% | 48% | 8% |
(1)NaOH ;NaAlO2 ;Na2CO3 ;Al(OH)3 ;Al2O3( 每空2分)
(2) 1.8 t(2分); 0.069 t(3分)
(2) 1.8 t(2分); 0.069 t(3分)
试题分析:(1)使用逆推法,电解得铝可知,E为氧化铝,D为氢氧化铝,而B处与二氧化碳发生双水解反应得氢氧化铝,可知C为碳酸钠,A为氢氧化钠。
(2)根据铝土矿中氧化铝的质量分数为55%,所以每生产1t纯净的氧化铝,需铝土矿的质量1/55%=1.8t。再根据反应方程式即可得苛性钠的质量为0.069 t。
点评:本题涉及工业获得金属铝的实验方案知识,是一道工业生产和化学结合的题目,其中工艺流程推断结合化学反应原理,以及铝的化合物性质可以顺利推出,后面的计算也只需要带入方程计算。

练习册系列答案
相关题目