题目内容
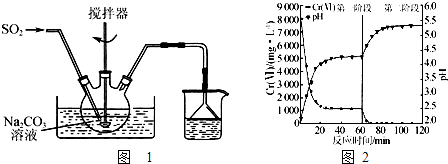
【题目】(1)请写出实验室制备Fe(OH)3胶体的离子方程式_______________;
请写出Cl2通入到澄清石灰水中的离子方程式_______________。
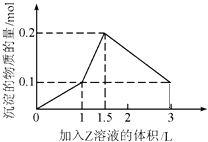
(2)向Ba(OH)2溶液中通入少量二氧化碳,请写出发生反应的离子方程式_______________。
(3)写出NH4HSO4 在水溶液中的电离方程式_______________;及其与NH4HCO3 在溶液中反应的离子方程式_____________________。
(4)写出过氧化钠与水反应的离子方程式:___________________________________。
(5)已知胃酸的主要成分是盐酸,请写出用小苏打片治疗胃酸过多的离子方程式______________;
如果病人同时患有胃溃疡,此时最好服用胃舒平【主要成分为Al(OH)3】,请写出相应的的离子方程式
_____________________________________
【答案】 Fe3+ +3H2O ![]() Fe(OH)3(胶体)+3H+ Cl2+ 2OH-= Cl-+ClO-+H2O CO2+ Ba2++2OH-=BaCO3↓+2H2O NH4HSO4=NH4++H++SO42- H++HCO3-=H2O+CO2↑ 2Na2O2+2H2O=4Na++4OH-+O2↑ HCO3-+H+=CO2↑+H2O Al(OH)3+3H+=Al3++3H2O
Fe(OH)3(胶体)+3H+ Cl2+ 2OH-= Cl-+ClO-+H2O CO2+ Ba2++2OH-=BaCO3↓+2H2O NH4HSO4=NH4++H++SO42- H++HCO3-=H2O+CO2↑ 2Na2O2+2H2O=4Na++4OH-+O2↑ HCO3-+H+=CO2↑+H2O Al(OH)3+3H+=Al3++3H2O
【解析】(1)三价铁离子水解生成氢氧化铁胶体和氢离子,离子方程式:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+,Cl2通入到澄清石灰水中反应生成氯化钙、次氯酸钙和水,反应的离子方程式为Cl2+ 2OH-= Cl-+ClO-+H2O,故答案为:Fe3++3H2O
Fe(OH)3(胶体)+3H+,Cl2通入到澄清石灰水中反应生成氯化钙、次氯酸钙和水,反应的离子方程式为Cl2+ 2OH-= Cl-+ClO-+H2O,故答案为:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+;Cl2+ 2OH-= Cl-+ClO-+H2O;
Fe(OH)3(胶体)+3H+;Cl2+ 2OH-= Cl-+ClO-+H2O;
(2)向Ba(OH)2溶液中通入少量二氧化碳,反应生成碳酸钡沉淀,反应的离子方程式为CO2+ Ba2++2OH-=BaCO3↓+2H2O,故答案为:CO2+ Ba2++2OH-=BaCO3↓+2H2O;
(3)NH4HSO4在水溶液中的电离方程式为NH4HSO4=NH4++H++SO42-;其与NH4HCO3在溶液中反应生成硫酸铵和二氧化碳,反应的离子方程式为H++HCO3-=H2O+CO2↑,故答案为:NH4HSO4=NH4++H++SO42-;H++HCO3-=H2O+CO2↑;
(4)过氧化钠与水反应生成氢氧化钠和氧气,反应的离子方程式为:2Na2O2+2H2O=4Na++4OH-+O2↑,故答案为:2Na2O2+2H2O=4Na++4OH-+O2↑;
(5)小苏打为NaHCO3,胃酸中含盐酸,用小苏打治疗胃酸过多的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑,二氧化碳和水写化学式,离子反应为H++HCO3-═H2O+CO2↑,如果病人同时患有胃溃疡,此时最好服用胃舒平,盐酸与氢氧化铝反应生成氯化铝和水,离子方程式为Al(OH)3+3H+═Al3++3H2O,故答案为:H++HCO3-═H2O+CO2↑;Al(OH)3+3H+═Al3++3H2O。

 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案【题目】研究催化剂对化学反应有重要意义.为探究催化剂对双氧水分解的催化效果,某研究小组做了如下实验:
(1)甲同学欲用图所示实验来证明MnO2是H2O2分解反应的催化剂.该实验(填“能”或“不能”)达到目的,原因是 . 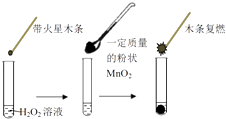
(2)为探究MnO2的量对催化效果的影响,乙同学分别量取50mL 1% H2O2加入容器中,
在一定质量范围内,加入不同质量的MnO2 , 测量所得气体体积,数据如下:
MnO2的质量/g | 0.1 | 0.2 | 0.4 |
40s末O2体积/mL | 49 | 61 | 86 |
由此得出的结论是 , 原因是 .
(3)为分析Fe3+和Cu2+对H2O2分解反应的催化效果,丙同学设计如下实验(三支试管中均盛有10mL 5% H2O2 ):
试管 | Ⅰ | Ⅱ | Ⅲ |
滴加试剂 | 5滴0.1molL﹣1FeCl3 | 5滴0.1molL﹣1 CuCl2 | 5滴0.3molL﹣1 NaCl |
产生气泡情况 | 较快产生细小气泡 | 缓慢产生细小气泡 | 无气泡产生 |
结论是 , 实验Ⅲ的目的是 .
(4)①查阅资料得知:将作为催化剂的FeCl3溶液加入H2O2溶液后,溶液中会发生两个氧化还原反应,且两个反应中H2O2均参加了反应,试从催化剂的角度分析,这两个
氧化还原反应的化学方程式分别是和(按反应发生的顺序写).
②在上述实验过程中,分别检测出溶液中有二价锰、二价铁和一价铜,由此得出选择作为H2O2分解反应的催化剂需要满足的条件是 .