题目内容
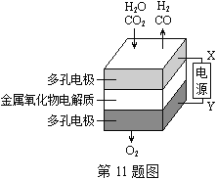
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )

A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移12mol 电子
3H2+CO,每消耗1molCH4转移12mol 电子
B. 电极A上H2参与的电极反应为:H2+2OH--2e-=2H2O
C. 电池工作时,CO32-向电极B移动
D. 电极B上发生的电极反应为:O2+2CO2+4e-=2CO32-
【答案】D
【解析】试题分析:A、1molCH4→CO,化合价由-4价→+2上升6价,1molCH4参加反应共转移6mol电子,错误; B、环境不是碱性,否则不会产生CO2,其电极反应式:CO+H2+2CO32--4e-=3CO2+H2O,错误;C、根据原电池工作原理,电极A是负极,电极B是正极,阴离子向负极移动,错误;D、根据电池原理,O2、CO2共同参加反应,其电极反应式:O2+2CO2+4e-=2CO32-,正确。

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目