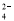题目内容
(1)相同质量的SO2、SO3的物质的量之比为____________;氧原子的个数之比为_ _______。
(2)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的摩尔质量是________;A的相对原子质量是____________;ACl2的化学式是__________。
(1)5∶4 5∶6 (2)95 g·mol-1 24 MgCl2
【解析】
试题分析:(1)根据 n=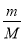 可知,相同质量的SO2、SO3的物质的量之比=
可知,相同质量的SO2、SO3的物质的量之比=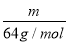 :
: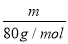 =5∶4;氧原子的个数之比=5×2∶4×3=5∶6。
=5∶4;氧原子的个数之比=5×2∶4×3=5∶6。
(2)19 g某二价金属氯化物(ACl2)中含有0.4 mol Cl-,则ACl2的物质的量=0.4mol÷2=0.2mol,因此根据n=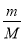 可知,该化合物的摩尔质量M=19.2g÷0.2mol=95 g/mol;氯元素的相对原子质量35.5,所以A的相对原子质量=95-35.5×2=24,因此A是Mg,则该化合物的化学式是MgCl2。
可知,该化合物的摩尔质量M=19.2g÷0.2mol=95 g/mol;氯元素的相对原子质量35.5,所以A的相对原子质量=95-35.5×2=24,因此A是Mg,则该化合物的化学式是MgCl2。
考点:考查物质的量的有关计算、化学式确定

练习册系列答案
相关题目