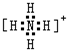题目内容
有X、Y、Z、W、M、N六种短周期元素,其中X、Y、Z、W同周期,Z与M、N与Y分别同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。
(1) 元素X与 M形成X2M2型化合物中阴阳离子个数比为:____________
(2) YM2晶体属于_____________晶体(填晶体类型);30g YM2晶体中含_________条共价键(阿伏加德罗常数用NA表示)
(3) 在工业上常用电解饱和XW的溶液来制碱。若用阴极室产生的气体为碱性燃料电池的燃料,则燃料电池中该气体所在电极为_______极,电极反应式为:_________________。
(4) 已知单质A为常见黑色固体粉末,B是元素Z的最高价含氧酸,其存在如图所示的转换关系:
(I) 若向C中滴加KSCN溶液立即呈血红色。则:常温下A在B的浓溶液中难以溶解的原因是 ;因此反应①的的条件是 。在工业上反应③是在___________(填设备)中进行的;在实验室用________(填药品名)检验D的存在;含D的尾气直接排放到大气中造成环境污染的后果是 ;
(II) 按要求写方程式:
写出反应②的化学方程式 ,
写出C与小苏打溶液反应的离子方程式 ,
(III) 若A是元素N的单质写出反应①的化学方程式:___________________。
(1)1:2 (2分)
(2)原子 (2分) 2NA (2分)
(3)负 (2分) H2-2e-+OH-=2H2O (2分)
(4)(Ⅰ) 钝化 加热 吸收塔 品红 形成酸雨 (各1分共5分)
(Ⅱ)2SO2+O2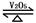 2SO3 (3分)
2SO3 (3分)
Fe3++3HCO3=Fe(OH)3↓+3CO2↑(3分)
(Ⅲ)C+2H2SO4(浓) 2SO2↑+CO2↑+2H2O (3分)
2SO2↑+CO2↑+2H2O (3分)
解析

| A、X、M两种元素只能形成X2M型化合物 | B、Y、Z两元素的气态氢化物中,Y的气态氢化物更稳定 | C、Z、W两元素的最高价氧化物对应水化物的酸性:Z>W | D、W、M两元素的某些单质或化合物可作为自来水消毒剂 |