题目内容
【题目】某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。
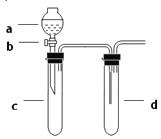
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是 __________________。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸,c中反应的化学方程式是________________。再由a向c中加2 mL蒸馏水,c中的实验现象是_________________。
(3)下表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是___________,理由是___________。
方案 | 反应物 |
甲 | Cu、浓 HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2,操作步骤为___________,实验现象为 __________,但此实验的不足之处是 _________________。
【答案】 检査装置气密性 Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O 反应变缓,气体颜色变淡 丙 耗酸量最少,无污染 向d中加入KBr溶液,c中加入固体KMnO4,由a向c中加入浓盐酸 c中有黄绿色气体产生,d中溶液变为黄棕色 没有处理尾气
【解析】考查实验设计与评价,(1)此操作步骤,是实验前进行的,因此此操作目的是检验装置气密性;(2)发生Cu和浓硝酸反应,即反应方程式为Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,加入蒸馏水,硝酸浓度降低,反应速率变换,铜和稀硝酸反应生成NO,因此气体颜色变浅;(3)甲:铜和浓硝酸反应生成NO2,NO2有毒,污染空气,不符合绿色化学理念;乙:铜和稀硝酸反应生成NO,NO有毒,污染空气,不符合绿色理念;丙:Cu和氧气反应生成CuO,CuO与稀硝酸反应生成硝酸铜和H2O,不产生污染物,消耗硝酸的量少,符合绿色理念;(4)向d中加入KBr溶液,c中加入固体KMnO4,由a向c中加入浓盐酸,c中发生2KMnO4+16HCl(浓)=2KCl+5Cl2↑+2MnCl2+8H2O,有氯气产生,现象是产生黄绿色气体,d中发生Cl2+2Br-=Br2+2Cl-,d中溶液变为黄棕色,氯气和液溴有毒,没有处理尾气装置。

 星级口算天天练系列答案
星级口算天天练系列答案