题目内容
【题目】如图,是实验室制备乙酸乙酯的装置。a试管中加入3 mL 95%的乙醇、2 mL 浓硫酸、2 mL 冰醋酸;b试管中是饱和碳酸钠溶液。连接好装置,用酒精灯对试管a加热,当观察到试管b中有明显现象时停止实验。
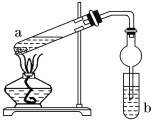
(1)在a试管中除了加入乙醇、浓硫酸和乙酸外,还应放入____________,目的是____________。
(2)试管b中观察到的主要现象是__________________________。
(3)实验中球形干燥管除起冷凝作用外,另一个重要作用是_________________。
(4)饱和Na2CO3溶液的作用是__________________________________________。
(5)反应结束后,将试管中收集到的产品倒入分液漏斗中,然后分液,得到乙酸乙酯。
【答案】沸石(或碎瓷片) 防止暴沸 溶液分层,在饱和碳酸钠溶液上层产生有特殊香味的无色液体 防止倒吸 除去乙酸和乙醇,降低乙酸乙酯的溶解度
【解析】
(1)还应放入沸石(或碎瓷片),目的是防止暴沸;
(2)碳酸钠溶液能溶解乙醇、与乙酸反应,但是乙酸乙酯不溶于饱和碳酸钠溶液,会分层;
(3)碳酸钠溶液能溶解乙醇、与乙酸反应,使压强减小;
(4)饱和碳酸钠溶液作用是除去乙酸和乙醇,降低乙酸乙酯的溶解度。
(1)在a试管中除了加入乙醇、浓硫酸和乙酸外,还应放入沸石(或碎瓷片),目的是防止暴沸;
(2)碳酸钠溶液能溶解乙醇、与乙酸反应,但是乙酸乙酯不溶于饱和碳酸钠溶液,会分层。则试管b中观察到的主要现象是:溶液分层,在饱和碳酸钠溶液上层产生有特殊香味的无色液体;
(3)酸钠溶液能溶解乙醇、与乙酸反应,使压强减小,则实验中球形干燥管除起冷凝作用外,另一个重要作用是防止倒吸;
(4)由以上分析可知,饱和Na2CO3溶液的作用是除去乙酸和乙醇,降低乙酸乙酯的溶解度。

【题目】下表列出了①~⑨九种元素在周期表中的位置。
族 | ⅠA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ | ||||
请按要求回答下列问题:
(1)①~⑨九种元素中非金属性最强的是________(填元素符号)。
(2)元素⑧的原子结构示意图是_________;由①、④、⑥三种元素组成的化合物,其电子式是_________。
(3)元素②、⑧的气态氢化物的稳定性较强的是________________(填化学式);元素③、⑨的最高价氧化物对应的水化物的酸性较强的是________________(填化学式)。
(4)③、④span>、⑧三种元素的原子半径由大到小的顺序是________________(填元素符号)。
(5)元素⑤、⑥组成的化合物的化学键类型是________________________。
(6)元素⑥的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应的水化物反应的离子方程式是________________
【题目】某温度时,两个恒容密闭容器中仅发生反应2NO2(g)2NO(g) +O2(g) ΔH > 0。实验测得:υ正(NO2)=k正c2(NO2),υ逆(NO)=k逆c2(NO)·c(O2),k正、k逆为化学反应速率常数,只受温度影响。
容器 编号 | 起始浓度(mol·L1) | 平衡浓度(mol·L1) | ||
c(NO2) | c(NO) | c(O2) | c(O2) | |
Ⅰ | 0.6 | 0 | 0 | 0.2 |
Ⅱ | 0.6 | 0.1 | 0 | |
下列说法不正确的是
A.Ⅰ中NO2的平衡转化率约为66.7%
B.Ⅱ中达到平衡状态时,c(O2)<0.2mol·L1
C.该反应的化学平衡常数可表示为![]()
D.升高温度,达到平衡状态时 Ⅰ中c(O2)<0.2mol·L1