题目内容
(10分)工业合成氨的反应: 是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量.
是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量.
⑴相同条件下,1 mol N2和3 mol H2所具有的能量 (“大于”、“小于”、“等于”)2 molNH3具有的能量 ;
⑵如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量 (“大于”、“小于”、“等于”)上述数值,其原因是 ;
⑶实验室模拟工业合成氨时,在容器为2L的密闭容器内,反应经过10min后,生成10 mol NH3,则用N2表示的该反应速率为: ;
⑷一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是
a.正反应速率和逆反应速率相等 b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值 d.N2和H2的浓度相等
e. N2、H2和NH3的体积分数相等 f.反应达到最大限度
【答案】

【解析】

练习册系列答案
 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
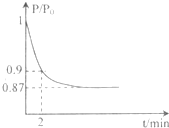 能源的开发利用与人类社会的可持续性发展息息相关.
能源的开发利用与人类社会的可持续性发展息息相关. 是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量.
是一个放热反应。已知该反应生成2molNH3时,放出92kJ的热量.