题目内容
有三种不同浓度的稀硫酸,体积比依次3∶2∶1,它们分别与等物质的量的K2CO3、KHCO3、Al刚好完全反应,此三种硫酸的物质的量浓度比为( )
| A.1∶1∶1 | B.6∶2∶3 |
| C.4∶3∶18 | D.2∶1∶3 |
C
设三种不同浓度H2SO4(aq)的体积分别为3 L、2 L、1 L。
K2CO3+H2SO4====K2SO4+H2O+CO2↑
1 mol 1 mol
1 mol c1(H2SO4)×3 L
2KHCO3+H2SO4====K2SO4+2H2O+2CO2↑
2 mol 1 mol
1 mol c2(H2SO4)×2 L
2Al+3H2SO4====Al2(SO4)3+3H2↑
2 mol 3 mol
1 mol c3(H2SO4)×1 L
c1(H2SO4)∶c2(H2SO4)∶c3(H2SO4)=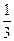 ∶
∶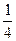 ∶
∶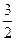 =4∶3∶18。
=4∶3∶18。
K2CO3+H2SO4====K2SO4+H2O+CO2↑
1 mol 1 mol
1 mol c1(H2SO4)×3 L
2KHCO3+H2SO4====K2SO4+2H2O+2CO2↑
2 mol 1 mol
1 mol c2(H2SO4)×2 L
2Al+3H2SO4====Al2(SO4)3+3H2↑
2 mol 3 mol
1 mol c3(H2SO4)×1 L
c1(H2SO4)∶c2(H2SO4)∶c3(H2SO4)=
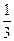 ∶
∶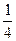 ∶
∶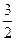 =4∶3∶18。
=4∶3∶18。
练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
 ∶
∶
 ∶
∶