题目内容
t℃时,在一密闭容器中充入2mol A和3mol B,发生如下化学反应:aA+B C+B(反应物、产物均为气体)平衡后测知各物质浓度有如下关系:{c(A)}a·c(B)=c(C)·c(D)然后在温度不变的情况下,扩大容器容积至原来10倍,结果A的百分含量始终未有改变,则这时B的转化率是
C+B(反应物、产物均为气体)平衡后测知各物质浓度有如下关系:{c(A)}a·c(B)=c(C)·c(D)然后在温度不变的情况下,扩大容器容积至原来10倍,结果A的百分含量始终未有改变,则这时B的转化率是
A.60% B.40% C.50% D.无法确定
B
【解析】
试题分析:平衡后测知各物质浓度有如下关系:{c(A)}a·c(B)=c(C)·c(D),则根据平衡常数表达式K=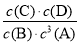 可知,K=1。在温度不变的情况下,扩大容器容积至原来10倍,结果A的百分含量始终未有改变,这说明平衡不变,因此反应前后体积不变,则a=1,所以
可知,K=1。在温度不变的情况下,扩大容器容积至原来10倍,结果A的百分含量始终未有改变,这说明平衡不变,因此反应前后体积不变,则a=1,所以
A + B C + B
C + B
起始量(mol) 2 3 0 0
转化量(mol)x x x x
平衡量(mol)2-x 3-x x x
由于反应前后体积不变,所以可以用物质的量代替浓度进行平衡常数计算
则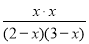 =1
=1
解得x=1.2
所以B的转化率=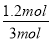 ×100%=40%,答案选B。
×100%=40%,答案选B。
考点:考查平衡常数、转化率的计算

练习册系列答案
相关题目