题目内容
一种由氯化铵制取氯气的工艺原理如下:
反应Ⅰ.2NH4Cl+MgO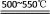 2NH3↑+MgCl2+H2O↑
2NH3↑+MgCl2+H2O↑
反应Ⅱ.2MgCl2+O2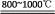 2MgO+2Cl2
2MgO+2Cl2
下列说法正确的是
A. 该工艺中MgO可循环利用
B. 理论上 1mol NH4Cl制得Cl2的体积一定为11.2L
C. 在800~1000℃条件下,O2的还原性强于Cl2的还原性
D. 若反应2NH3+MgCl2+H2O=2NH4Cl+MgO能自发进行,则该反应ΔH>0
练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目



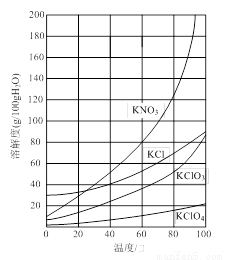
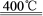 3KClO4 +KCl;2KClO3
3KClO4 +KCl;2KClO3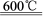 2KCl+3O2↑。实验室可用KClO3制备高纯KClO4固体,实验中必须使用的用品有:热过滤装置(如下图所示)、冰水。
2KCl+3O2↑。实验室可用KClO3制备高纯KClO4固体,实验中必须使用的用品有:热过滤装置(如下图所示)、冰水。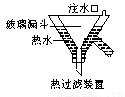
 2H++CO32-
2H++CO32-