题目内容
黄铁矿(FeS2)燃烧产生的SO2通过下列工艺过程既能制得H2SO4,又能制得H2。
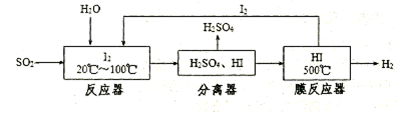
(1)该过程中能循环利用的物质为 。
(2)在该过程中,使用膜反应器及时分离出HI分解产生的H2,目的是 (用平衡移动的原理解释)。
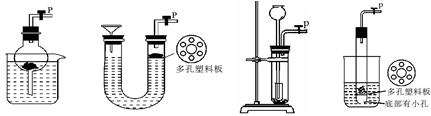
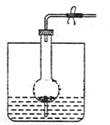
(3)某研究性学习小组欲探究SO2能否与BaCl2溶液反应生成BaSO3沉淀,进行如下实验。已知浓硫酸的沸点为338℃,加热时酒灯火焰的温度为400℃~500℃。
①甲同学用装置I进行实验,发现BaCl2溶液中出现白色沉淀,且白色沉淀不溶于盐酸,请解释生成该白色沉淀的可能原因 (用离子方程式表示)。
②乙同学认为甲同学的装置不完善,设计了改进装置II进行实验(夹持装置和A中加热装置已略,气密性已检查)。
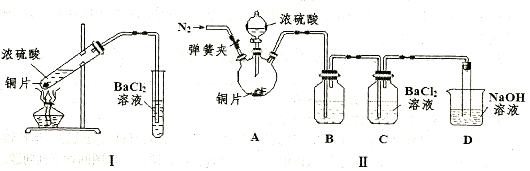
a.打开弹簧夹通入N2,一段时间后关闭弹簧夹;b.滴加一定量浓硫酸,加热A,一段时间后C中未见沉淀生成。操作a的目的是 ,装置B中的剂是 。
③丙同学取乙实验后的C中溶液少许,滴加一种无色溶液,产生不溶于盐酸的白色沉淀,丙同学滴加的试剂可能是 (填字母编号)。
a.NaOH溶液 b.H2O2溶液 c.新制氯水 d.酸性KmnO4溶液
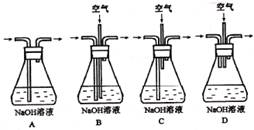
④装置D中与导管连接的是硬质玻璃管,则装置D的作用是 。

(1)该过程中能循环利用的物质为 。
(2)在该过程中,使用膜反应器及时分离出HI分解产生的H2,目的是 (用平衡移动的原理解释)。
(3)某研究性学习小组欲探究SO2能否与BaCl2溶液反应生成BaSO3沉淀,进行如下实验。已知浓硫酸的沸点为338℃,加热时酒灯火焰的温度为400℃~500℃。
①甲同学用装置I进行实验,发现BaCl2溶液中出现白色沉淀,且白色沉淀不溶于盐酸,请解释生成该白色沉淀的可能原因 (用离子方程式表示)。
②乙同学认为甲同学的装置不完善,设计了改进装置II进行实验(夹持装置和A中加热装置已略,气密性已检查)。

a.打开弹簧夹通入N2,一段时间后关闭弹簧夹;b.滴加一定量浓硫酸,加热A,一段时间后C中未见沉淀生成。操作a的目的是 ,装置B中的剂是 。
③丙同学取乙实验后的C中溶液少许,滴加一种无色溶液,产生不溶于盐酸的白色沉淀,丙同学滴加的试剂可能是 (填字母编号)。
a.NaOH溶液 b.H2O2溶液 c.新制氯水 d.酸性KmnO4溶液
④装置D中与导管连接的是硬质玻璃管,则装置D的作用是 。
(1)I2 (2分)
(2)使平衡向正反应方向移动,提高产物的产率。(2分)
(3)① SO42-+Ba2+=BaSO4↓或2Ba2++2SO2+O2+2H2O=2BaSO4↓+4H+(2分,答对一个即给分)
② 排出装置中的O2(2分) 饱和NaHSO3溶液(2分)
③ b(2分) ④吸收尾气并防倒吸(2分)
试题分析:(1)由工艺流程可知能循环利用的物质为I2。(2)及时分离出HI分解产生的H2,使HI的分解平衡向正反应方向移动,提高了I2和H2的产率。(3)本小题首先抓住已知信息“浓硫酸的沸点为338 ℃,加热时酒精灯火焰的温度为400℃~500℃”,说明浓硫酸在温度较高时也能挥发出H2SO4蒸气。①白色沉淀应为BaSO4,可能原因有二:一是挥发出的H2SO4提供的SO42-与Ba2+反应生成,二是空气中O2的氧化所致。②操作a通入N2目的是排出装置中的O2。C中未见沉淀生成,说明B中的试剂能吸收挥发出的H2SO4且不产生新的杂质,还不能与SO2反应,故该试剂应是饱和NaHSO3溶液。③乙实验后的C中的溶液会溶有SO2,题中不溶于盐酸的白色沉淀应是BaSO4,滴加一种无色溶液, 只能是H2O2溶液。④装置D的作用是既能吸收未反应的SO2防止大气污染,又能防止NaOH溶液倒吸入装置C中影响实验结果。2的性质为载体的实验题,涉及化学平衡的移动原理的考查。

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目

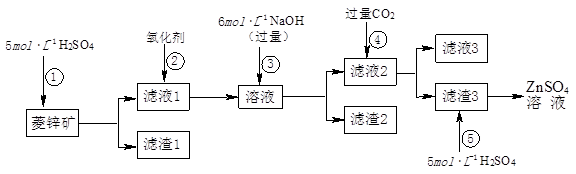
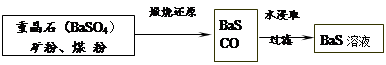


 。
。 CoO2+LiC6,写出该电池放电时的正极反应式 。
CoO2+LiC6,写出该电池放电时的正极反应式 。