题目内容
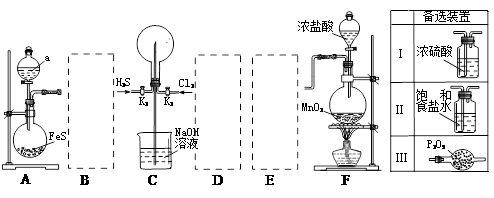
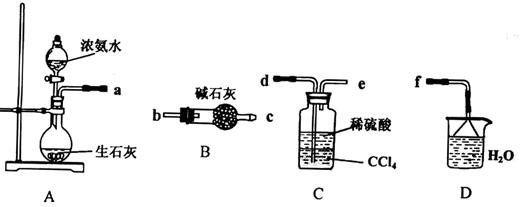
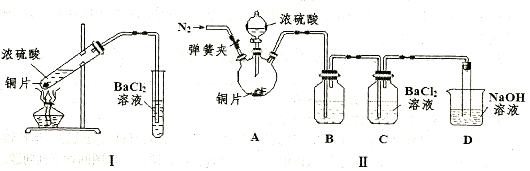
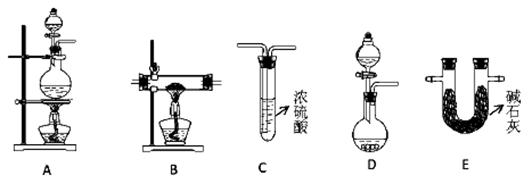
下图所示为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去),请根据要求完成下列各题(仪器装置可任意选用,必要时可重复选择,a、b为活塞)。

(1)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为 (填代号)。能验证CO氧化产物的现象是 。
(2)停止CO和CO2混合气体的通入,E内放置Na2O2,按A→E→D→B→H装置顺序制取纯净干燥的O2,并用O2氧化乙醇。此时,活塞a应 ,活塞b应 ,需要加热的仪器装置有 (填代号),m中反应的化学方程式为: 。
(3)若气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,按A→G→E→D装置顺序制取干燥的氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有 。
②实验中观察到E内有红棕色气体出现,证明氨气具有 性。

(1)若气体入口通入CO和CO2的混合气体,E内放置CuO,选择装置获得纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为 (填代号)。能验证CO氧化产物的现象是 。
(2)停止CO和CO2混合气体的通入,E内放置Na2O2,按A→E→D→B→H装置顺序制取纯净干燥的O2,并用O2氧化乙醇。此时,活塞a应 ,活塞b应 ,需要加热的仪器装置有 (填代号),m中反应的化学方程式为: 。
(3)若气体入口改通空气,分液漏斗内改加浓氨水,圆底烧瓶内改加NaOH固体,E内放置铂铑合金网,按A→G→E→D装置顺序制取干燥的氨气,并验证氨的某些性质。
①装置A中能产生氨气的原因有 。
②实验中观察到E内有红棕色气体出现,证明氨气具有 性。
(1)ACBECF(2分) AB之间的C装置中溶液保持澄清,EF之间的C装置中溶液变浑浊。(2分)(2)关闭(1分) 打开(1分) k和m(2分) 2CH3CH2OH+O2 2CH3CHO+2H2O (2分)(3) ①氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度降低而放出;氢氧化钠吸水,促使氨气放出;氢氧化钠电离出的OH-增大了氨水中的OH-浓度,使氨的电离平衡左移,促使氨气放出。(3分)②还原(1分)
2CH3CHO+2H2O (2分)(3) ①氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度降低而放出;氢氧化钠吸水,促使氨气放出;氢氧化钠电离出的OH-增大了氨水中的OH-浓度,使氨的电离平衡左移,促使氨气放出。(3分)②还原(1分)
 2CH3CHO+2H2O (2分)(3) ①氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度降低而放出;氢氧化钠吸水,促使氨气放出;氢氧化钠电离出的OH-增大了氨水中的OH-浓度,使氨的电离平衡左移,促使氨气放出。(3分)②还原(1分)
2CH3CHO+2H2O (2分)(3) ①氢氧化钠溶于水放出大量热,温度升高,使氨的溶解度降低而放出;氢氧化钠吸水,促使氨气放出;氢氧化钠电离出的OH-增大了氨水中的OH-浓度,使氨的电离平衡左移,促使氨气放出。(3分)②还原(1分)试题分析:(1)用A装置的NaOH来除CO中混有的CO2,(生成Na2CO3),用C装置检验有没有除尽CO2,B装置是干燥气体的,纯净的CO,通入E中,生成的CO2能使装置C有沉淀,多余的CO在装置F处尾气吸收。
(2)关闭装置A的活塞a,停止通入CO和CO2,打开活塞b,使稀硫酸和A中的碳酸钠反应,产生CO2,通入E,和Na2O2,产生O2,用D吸收O2混有的CO2,用B干燥O2中的H2O,纯净的O2在H中和乙醇发生催化氧化反应。加热k产生乙醇蒸汽,加热m ,是因为乙醇催化氧化需要催化剂铜和加热条件。
(3)这过程发生的反应为4NH3+5O2=4NO+6H2O(NH3表现还原性);2NO+O2=2NO2(红棕色)。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目