题目内容
【题目】铝-石墨双离子电池是一种高效电池。原理为:AlLi + Cx(PF6)![]() Al+xC+Li++PF6-,电池结构如图所示。下列说法正确的是
Al+xC+Li++PF6-,电池结构如图所示。下列说法正确的是
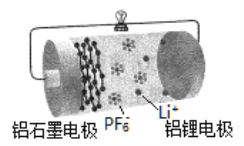
A. 放电时外电路中电子向铝锂电极移动
B. 放电时正极反应为Cx(PF6)+e-= xC+ PF6-
C. 充电时,铝石墨电极上发生还原反应
D. 以此电池为电源,电解NaCl饱和溶液,当生成11.2LH2时,电池负极质量减少7g
【答案】B
【解析】放电时铝锂电极中锂失电子作为负极,外电路中电子由负极铝锂电极向正极铝石墨移动,A错误;放电时正极铝石墨电极Cx(PF6)得电子产生PF6-,正极反应为Cx(PF6)+e-= xC+ PF6-,B正确;放电时,铝石墨电极上发生还原反应,充电时,铝石墨电极上发生氧化反应,C错误;电解NaCl饱和溶液,产生氯气和氢气,由于没有给出生成氢气的外界条件,无法计算出氢气的量,也就不能进行相关的计算,D错误;正确选项B。

练习册系列答案
 全能闯关100分系列答案
全能闯关100分系列答案
相关题目