题目内容
1918年,Lewis提出反应速率的碰撞理论:反应物分子间的相互碰撞是反应进行的必要条件,但并不是每次碰撞都能引起反应,只有少数碰撞才能发生化学反应。能引发化学反应的碰撞称之为有效碰撞。
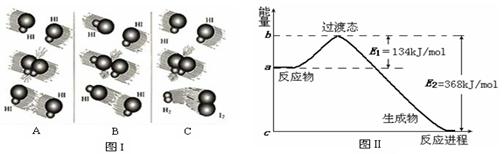
⑴ 图I是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是
(选填“A”、“B”或“C”);
⑵20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。
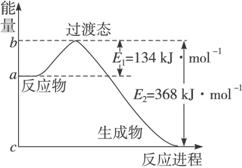
图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式: ;
⑶ 过渡态理论认为,催化剂改变反应速率的原因是改变了反应的途径,对大多数反应而言主要是通过改变过渡态而导致有效碰撞所需要的能量发生变化。请在图Ⅱ中作出NO2和CO反应时使用催化剂而使反应速率加快的能量变化示意图;
⑴ C;
⑵ NO2(g)+CO(g)=CO2(g)+NO(g);ΔH=-234kJ·mol-1 ;
⑶ (见下图)

解析:
⑴碰撞是否有效,关键看有无新物质生成,由图I可知,只有C发生的碰撞
生成了H2和I2,为有效碰撞。
⑵ΔH=E(生成物-)E(反应物),与反应过程无关,图Ⅱ中虽没有给出E(生成物)
和E(反应物)的数值,但其差值可通过E1、E2计算出,即ΔH=-(E2-E1)。
⑶由题意知:使用催化剂加快反应速率主要是通过改变过渡态的能量,使有效碰撞容易
发生,实际上是降低了过渡态的能量,应注意的是使用催化剂并未改变反应物、生成物的能量。

 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案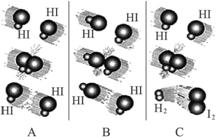
图Ⅰ
图Ⅱ
(1)图Ⅰ是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是__________(选填“A”“B”或“C”);
(2)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。图 Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:_______________________________________________________。
(3)进一步研究表明,化学反应的能量变化(ΔΗ)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键时所需吸收的能量。下表是部分化学键的键能数据:
化学键 | P—P | P—O | O==O | P==O |
键能/kJ·mol-1 | 197 | 360 | 499 | x |
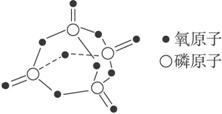
已知白磷的燃烧热为2 378.0 kJ·mol-1,白磷完全燃烧的产物结构如图Ⅲ所示,则上表中x=_____________。
图Ⅲ

图Ⅰ
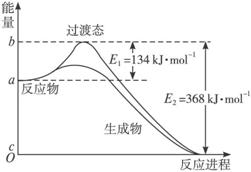
图Ⅱ
(1)图Ⅰ是HI分解反应中HI分子之间的几种碰撞示意图,其中属于有效碰撞的是_______(选填“A”“B”或“C”)。
(2)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。
图Ⅱ是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:___________________________。
(3)过渡态理论认为,催化剂改变反应速率的原因是改变了反应的途径,对大多数反应而言主要是通过改变过渡态而导致有效碰撞所需要的能量发生变化。请在图Ⅱ中作出NO2和CO反应时使用催化剂而使反应速率加快的能量变化示意图。
(4)进一步研究表明,化学反应的能量变化(ΔH)与反应物和生成物的键能有关。键能可以简单地理解为断开1 mol化学键时所需吸收的能量。下表是部分化学键的键能数据:
化学键 | P—P | P—O | O=O | P=O |
键能/kJ·mol-1 | 197 | 360 | 499 | X |

图Ⅲ
已知白磷的燃烧热为2 378.0 kJ·mol-1,白磷完全燃烧的产物结构如图Ⅲ所示,则上表中X=_________。


