题目内容
I.科学家一直致力于“人工固氮”的新方法研究。
(l)目前合成氨技术原理为:![]() △
△![]()
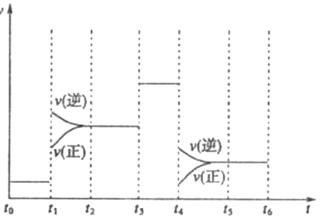 下图表示工业合成氨反应在某一段时间中反应速率与反应过程的关系曲线图:
下图表示工业合成氨反应在某一段时间中反应速率与反应过程的关系曲线图:
①氢化物的体积分数最高的一段时间为 ;![]() 时刻改变的反应条件是 。
时刻改变的反应条件是 。
②![]() 极易溶于水,其水溶液俗称氨水。用水稀释
极易溶于水,其水溶液俗称氨水。用水稀释![]() 的氨水,溶液中随着水量的增加而减小的是 (填序号)。
的氨水,溶液中随着水量的增加而减小的是 (填序号)。
![]()
![]()
![]()
![]()
(2)1998年希腊亚里士多德大学的两位科学家采用高质子导电性的SCY冉瓷(能传递![]() ),实现了高温常压下利用
),实现了高温常压下利用![]() 和
和![]() 电解合成氨。其阴极的电极反应式 。
电解合成氨。其阴极的电极反应式 。
(3)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,![]() 在催化剂(掺有少量
在催化剂(掺有少量![]() 的
的![]() )表面与水发生下列反应:
)表面与水发生下列反应:
![]() △
△![]() 进一步研究
进一步研究![]() 生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表
生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表
| 303 | 313 | 323 |
| 4.8 | 5.9 | 6.0 |
①此合成反应的![]() 0,△
0,△![]() 0,(填“>”“<”或“=”)。
0,(填“>”“<”或“=”)。
②已知:![]() △
△![]() ;
;
![]() △
△![]()
则![]() △
△![]() = 。
= 。
II.已知可逆反应![]() (未配平)△
(未配平)△![]() 。温度为
。温度为![]() 时,在容积固定的容器中发生反应,各物质的浓度随时间变化的关系如图
时,在容积固定的容器中发生反应,各物质的浓度随时间变化的关系如图![]() 所示。
所示。
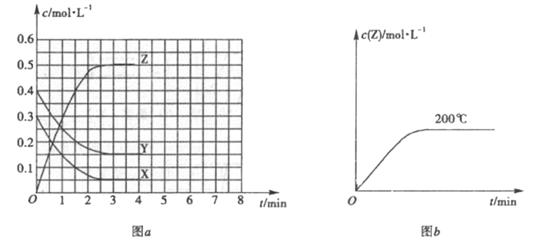
(1)![]() ℃时,该反应的平衡常数为
℃时,该反应的平衡常数为
(2)图![]() 为200℃时容器内
为200℃时容器内![]() 的变化曲线,请在图中补画该反应在100℃时的
的变化曲线,请在图中补画该反应在100℃时的![]() 的
的
变化曲线。
Ⅰ. (l)①![]() (2分) 升温(2分) ②bd(2分)
(2分) 升温(2分) ②bd(2分)
(2) ![]() (2分)
(2分)
(3)①>,>(2分) ②+l530![]() (2分)
(2分)
II.(1)33. 3(2分) (2)(2分)

(14分)I.科学家一直致力于“人工固氮”的新方法研究。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2 (g)+6H2O (l)4NH3 (g)+3O2 (g) ΔH= a kJ·mol-1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| 温度 T/K | 303 | 313 | 323 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
① 此合成反应的a 0 (填“>”“<”或“=”)
② 已知:
N2 (g) + 3H2(g)2NH3 (g) ΔH=-92.4 kJ·mol-1,
2H2 (g)+ O2 (g)===2H2O (l) ΔH=-571.6 kJ·mol-1,
则2N2 (g) + 6H2O (l)4NH3 (g) + 3O2 (g) ΔH= ;
(2)用水稀释0.1 mol·L-1氨水,溶液中随着水量的增加而减小的是 (填字母标号)
II.工业生产中产生含SO2的废气,经石灰吸收和氧化后制成硫酸钙,硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、水泥等。
(1)硫酸生产中,SO2催化氧化成SO3的热化学方程式为:
2SO2 (g) + O2(g)2SO3 (g) ΔH=-196.0 kJ·mol-1
① 容器体积不变时,为了提高SO2的转化率,可采用的措施是 (填字母标号)
A.加入V2O5作催化剂 B.使用过量SO2 C.高温 D.通入过量空气
② 某温度时,在一个容积为10L的密闭容器中充入4.0 molSO2和2.0 molO2,半分钟后达到平衡,并放出352.8kJ的热量。此时SO2的转化率是 ,该温度下的平衡常数K= ;
(2)已知25℃时,Ksp(CaSO4)=7.10×10-5。向0.100 L 含CaSO4固体的溶液中加入2.22 gCaCl2 粉末充分搅拌,假设溶液的体积变化忽略不计,则溶液中CaSO4固体的质量将 (填“增大”、“减小”或“不变”,下同),Ksp(CaSO4)将 。
(14分)I.科学家一直致力于“人工固氮”的新方法研究。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2 (g)+6H2O(l) 4NH3 (g)+3O2 (g) ΔH=a kJ·mol-1
4NH3 (g)+3O2 (g) ΔH=a kJ·mol-1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| 温度T/K | 303 | 313 | 323 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
 ”“<”或“=”)
”“<”或“=”)②已知:
N2 (g) + 3H2(g)
 2NH3 (g) ΔH=-92.4kJ·mol-1,
2NH3 (g) ΔH=-92.4kJ·mol-1,2H2 (g) + O2 (g)===2H2O (l) ΔH=-571.6kJ·mol-1,
则2N2 (g) + 6H2O(l)
 4NH3 (g) + 3O2 (g) ΔH= ;
4NH3 (g) + 3O2 (g) ΔH= ;(2)用水稀释0.1 mol·L-1氨水,溶液中随着水量的增加而减小的是 (填字母标号)
II.工业生产中产生含SO2的废气,经石灰吸收和氧化后制成硫酸钙,硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、水泥等。
(1)硫酸生产中,SO2催化氧化成SO3的热化学方程式为:
2SO2 (g) + O2(g)
 2SO3 (g) ΔH=-196.0kJ·mol-1
2SO3 (g) ΔH=-196.0kJ·mol-1①容器体积不变时,为了提高SO2的转化率,可采用的措施是 (填字母标号)
| A.加入V2O5作催化剂 | B.使用过量SO2 | C.高温 | D.通入过量空气 |
(2)已知25℃时,Ksp(CaSO4)=7.10×10-5。向0.100 L 含CaSO4固体的溶液中加入2.22 gCaCl2 粉末充分搅拌,假设溶液的体积变化忽略不计,则溶液中CaSO4固体的质量将 (填“增大”、“减小”或“不变”,下同),Ksp(CaSO4)将 。
(14分)I.科学家一直致力于“人工固氮”的新方法研究。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2 (g)+6H2O (l) 4NH3 (g)+3O2 (g) ΔH= a kJ·mol-1
4NH3 (g)+3O2 (g) ΔH= a kJ·mol-1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
|
温度 T/K |
303 |
313 |
323 |
|
NH3生成量/(10-6 mol) |
4.8 |
5.9 |
6.0 |
① 此合成反应的a 0 (填“>”“<”或“=”)
② 已知:
N2 (g) + 3H2(g) 2NH3 (g) ΔH=-92.4 kJ·mol-1,
2NH3 (g) ΔH=-92.4 kJ·mol-1,
2H2 (g) + O2 (g)===2H2O (l) ΔH=-571.6 kJ·mol-1,
则2N2 (g) + 6H2O (l) 4NH3 (g) + 3O2 (g) ΔH=
;
4NH3 (g) + 3O2 (g) ΔH=
;
(2)用水稀释0.1 mol·L-1氨水,溶液中随着水量的增加而减小的是 (填字母标号)

II.工业生产中产生含SO2的废气,经石灰吸收和氧化后制成硫酸钙,硫酸钙是一种用途非常广泛的产品,可用于生产硫酸、水泥等。
(1)硫酸生产中,SO2催化氧化成SO3的热化学方程式为:
2SO2 (g) + O2(g) 2SO3 (g) ΔH=-196.0 kJ·mol-1
2SO3 (g) ΔH=-196.0 kJ·mol-1
① 容器体积不变时,为了提高SO2的转化率,可采用的措施是 (填字母标号)
A.加入V2O5作催化剂 B.使用过量SO2 C.高温 D.通入过量空气
② 某温度时,在一个容积为10L的密闭容器中充入4.0 molSO2和2.0 molO2,半分钟后达到平衡,并放出352.8kJ的热量。此时SO2的转化率是 ,该温度下的平衡常数K= ;
(2)已知25℃时,Ksp(CaSO4)=7.10×10-5。向0.100 L 含CaSO4固体的溶液中加入2.22 gCaCl2 粉末充分搅拌,假设溶液的体积变化忽略不计,则溶液中CaSO4固体的质量将 (填“增大”、“减小”或“不变”,下同),Ksp(CaSO4)将 。
I.科学家一直致力于“人工固氮”的新方法研究。
(1)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生下列反应:2N2 (g)+6H2O (l)![]() 4NH3 (g)+3O2 (g) ΔH= a kJ·mol-1
4NH3 (g)+3O2 (g) ΔH= a kJ·mol-1
进一步研究NH3生成量与温度的关系,常压下达到平衡时测得部分实验数据如下表:
| 温度 T/K | 303 | 313 | 323 |
| NH3生成量/(10-6 mol) | 4.8 | 5.9 | 6.0 |
 (2010?聊城二模)I.科学家一直致力于“人工固氮”的新方法研究.
(2010?聊城二模)I.科学家一直致力于“人工固氮”的新方法研究.