题目内容
下列A~D四组,每组有两个反应,其中两个反应可用同一个离子方程式表示的是( )
| | (Ⅰ) | (Ⅱ) |
| A | 少量SO2通入Ba(OH)2溶液中 | 过量SO2通入少量Ba(OH)2溶液中 |
| B | 少量浓氨水滴入Al2(SO4)3溶液中 | 少量Al2(SO4)3溶液滴入浓氨水中 |
| C | 0.1 mol Cl2通入含0.2 mol FeBr2的溶液中 | 0.3 mol Cl2通入含0.2 mol FeBr2的溶液中 |
| D | 过量BaCl2溶液与少量Na2SO4溶液相混合 | 少量Ba(OH)2溶液与过量MgSO4溶液相混合 |
B
解析

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
下列离子方程式中,正确的
| A.向AlCl3溶液中逐渐滴入NaOH溶液至过量:Al3++4OH-=AlO2-+2H2O |
| B.将碳酸钙加入过量盐酸中:CO32-+2H+=CO2↑+H2O |
| C.向氯化铁溶液中加入铁粉:2Fe3++Fe=3Fe2+ |
| D.在CuSO4溶液中加入Ba(OH)2溶液:Ba2+ + SO42-= BaSO4↓ |
常温下,向0.25 mol·L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中不正确的是 ( )。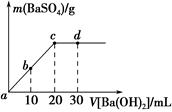
| A.硫酸溶液的体积为10 mL |
| B.b时刻溶液中SO42—的浓度约为0.125 mol·L-1 |
| C.d时刻溶液的pH为13 |
| D.溶液的导电能力:c<d<b<a |
甲、乙、丙是三种不含相同离子的可溶性强电解质。它们所含离子如表所示:
| 阳离子 | 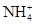 、Na+、Mg2+ 、Na+、Mg2+ |
| 阴离子 | OH-、 、 、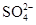 |
取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是( )
①MgSO4 ②NaOH ③(NH4)2SO4 ④Mg(NO3)2 ⑤NH4NO3
A.①② B.③④ C.③⑤ D.①⑤
下列离子方程式书写正确的是 ( )。
| A.澄清石灰水与少量小苏打溶液混合:Ca2++2OH-+2HCO3—=CaCO3↓+CO32—+2H2O |
| B.磁性氧化铁置于氢碘酸溶液中:Fe3O4+8HI=2Fe3++Fe2++4H2O+8I- |
| C.NaHSO4溶液中滴加过量Ba(OH)2溶液:H++SO42—+Ba2++OH-=BaSO4↓+H2O |
| D.醋酸与氨水混合:CH3COOH+NH3·H2O=CH3COONH4+H2O |
某混合物的水溶液,只可能含有以下离子中的若干种:Na+、NH4+、Ba2+、Cl-、CO32-、SO42-。现取两份200 mL溶液进行如下实验:①第一份加足量NaOH溶液,加热,收集到气体1.36 g;②第二份加足量BaCl2溶液后,得干燥沉淀12.54 g,经足量盐酸洗涤、干燥后,沉淀质量为4.66 g。根据上述实验事实,以下推测中正确的是( )
| A.一定不存在Ba2+,可能存在NH4+ |
| B.不可能存在Ba2+、Cl- |
| C.Na+一定存在,且c(Na+)≥0.2 mol/L |
| D.Na+、Cl-可能存在 |
下列分子或离子在指定的分散系中能大量共存的一组是( )
A.银氨溶液:Na+、K+、N 、NH3·H2O 、NH3·H2O |
| B.空气:C2H2、CO2、SO2、NO |
| C.氢氧化铁胶体:H+、K+、S2-、Br- |
D.高锰酸钾溶液:H+、Na+、S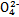 、葡萄糖分子 、葡萄糖分子 |
某同学对下列相应反应的离子方程式所作的评价,其中合理的是( )
| 选项 | 化学反应 | 离子方程式 | 评价 |
| A | 碳酸氢钠的水解 | HC +H2O +H2O H3O++C H3O++C | 正确 |
| B | NaHCO3溶液中滴入NaOH溶液 | HC +OH- +OH- CO2↑+H2O CO2↑+H2O | 错误,电荷不守恒 |
| C | “84消毒液”(有效成分为NaClO溶液)和“洁厕灵”(有效成分为浓盐酸)混合放出氯气 | ClO-+Cl-+H+ Cl2↑+OH- Cl2↑+OH- | 正确 |
| D | 少量的FeBr2与过量Cl2反应 | 2Fe2++2Br-+2Cl2 2Fe3++Br2+4Cl- 2Fe3++Br2+4Cl- | 错误,Fe2+与Br-的物质的量之比与化学式不符 |
