题目内容
【题目】下列说法正确的是
A. NaCl溶于水与加热熔化时破坏的作用力不同
B. NH5的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,是既具有离子键又具有共价键的离子化合物
C. 现代科技已经能够拍到氢键的“照片”,直观地证实了水分子间的氢键是一个水分子中的氢原子与另一个水分子中的氧原子间形成的化学键
D. SiO2分子是由1个Si原子和两个O原子构成的原子晶体
【答案】B
【解析】A、NaCl溶于水与加热熔化时破坏的作用力相同,均是离子键,A错误;B、NH5的所有原子的最外层都符合相应的稀有气体原子的最外层电子结构,电子式为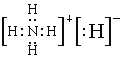 ,因此是既具有离子键又具有共价键的离子化合物,B正确;C、氢键不是化学键,C错误;D、SiO2晶体是Si原子和O原子按照1:2构成的空间网状结构的原子晶体,不存在分子,D错误,答案选B。
,因此是既具有离子键又具有共价键的离子化合物,B正确;C、氢键不是化学键,C错误;D、SiO2晶体是Si原子和O原子按照1:2构成的空间网状结构的原子晶体,不存在分子,D错误,答案选B。

练习册系列答案
 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
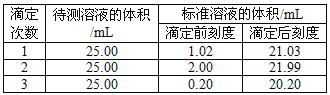
【题目】已知1,2-二溴乙烷的主要物理性质如表:
熔点 | 沸点 | 密度 | 溶解性 |
9.79°C | 131.4°C | 2.18g/cm3 | 难溶于水,易溶于醇、醚等 |
如图为实验室用乙烯与液溴作用制取1,2-二溴乙烷的部分装置图:

(1)A、C中都盛有水,这两个装置的作用分别是______________、______________;
(2)B和D装置都盛有NaOH溶液,它们的作用分别是______________、______________;
(3)试写出以乙醇、浓硫酸、液溴为主要原料生成1,2-二溴乙烷的主要化学反应方程式_____________。