题目内容
下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
(1)④、⑥、⑦的离子半径由大到小的顺序为 。
(2)1971年美国科学家通过细冰获得含元素④的含氧酸(HXO),在与水反应时,两种分子中的共价键分别断裂成两部分,再重新组合,写出该反应的化学方程式 。
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为 。在酸性溶液中该物质能将Fe2+氧化,写出该反应的离子方程式 。
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气
体,D溶液显碱性。
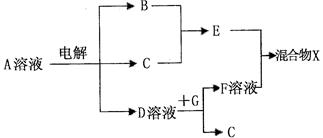
①写出D溶液与G反应的化学方程式 。
②常温下,若电解l L 0.1 mol/L A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为 mol。
③若仅电解l L 0.1 mol/L A溶液,图中各步反应均为完全转化,而各物质在反应过程中没有损耗,则混合物X中含有的物质有 。
| | ⅠA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | | | ② | ④ | |
| 3 | ⑤ | | ③ | | | ⑥ | ⑦ | |
(2)1971年美国科学家通过细冰获得含元素④的含氧酸(HXO),在与水反应时,两种分子中的共价键分别断裂成两部分,再重新组合,写出该反应的化学方程式 。
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为 。在酸性溶液中该物质能将Fe2+氧化,写出该反应的离子方程式 。
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气
体,D溶液显碱性。

①写出D溶液与G反应的化学方程式 。
②常温下,若电解l L 0.1 mol/L A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为 mol。
③若仅电解l L 0.1 mol/L A溶液,图中各步反应均为完全转化,而各物质在反应过程中没有损耗,则混合物X中含有的物质有 。
(1)S2->Cl->F-(1分)
(2)HFO+H2O=HF+H2O2(2分)
(3) (2分)
(2分)
H2O2+2Fe2++2H+=2Fe3++2H2O(2分)
(4)①2Al+2NaOH+2H2O=2NaAlO2+3H2↑(2分)
②0.01(1分)
③Al(OH)3 H2O、NaCl(答对Al(OH)3给1分,全对给2分)
(2)HFO+H2O=HF+H2O2(2分)
(3)
 (2分)
(2分)H2O2+2Fe2++2H+=2Fe3++2H2O(2分)
(4)①2Al+2NaOH+2H2O=2NaAlO2+3H2↑(2分)
②0.01(1分)
③Al(OH)3 H2O、NaCl(答对Al(OH)3给1分,全对给2分)
略

练习册系列答案
相关题目
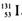 。
。 发射的
发射的 射线可杀伤一部分甲状腺细胞,医疗上常采用其治疗甲状腺机能亢进。但直接受到大剂量辐射时会出现细胞变异,甚至形成恶性肿瘤。下列有关
射线可杀伤一部分甲状腺细胞,医疗上常采用其治疗甲状腺机能亢进。但直接受到大剂量辐射时会出现细胞变异,甚至形成恶性肿瘤。下列有关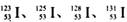 的说法中正确的是
的说法中正确的是 是同一种核素
是同一种核素 然同位素的相对原子质量与这些同位素所占的一定百分比计算出的平均值
然同位素的相对原子质量与这些同位素所占的一定百分比计算出的平均值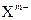 、
、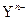 核外电子层结构相同,则关于X、Y两元素的叙述正确的是
核外电子层结构相同,则关于X、Y两元素的叙述正确的是
 数52,中子数28,其基态原子未成对电子数为
数52,中子数28,其基态原子未成对电子数为