题目内容
下列排列顺序中,正确的是( )
①热稳定性:HF>HCl>HBr>HI
②离子半径:Na+>Mg2+>F-
③密度:四氯化碳>己烷>水
④结合质子能力:OH->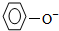 >HCO3-.
>HCO3-.
①热稳定性:HF>HCl>HBr>HI
②离子半径:Na+>Mg2+>F-
③密度:四氯化碳>己烷>水
④结合质子能力:OH->
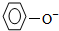 >HCO3-.
>HCO3-.分析:①同主族自上而下非金属性减弱,非金属性越强氢化物越稳定;
②电子层结构相同核电荷数越大离子半径越小;
③四氯化碳密度比水大,己烷密度比水小;
④酸性越强,离子的结构质子的能力越弱.
②电子层结构相同核电荷数越大离子半径越小;
③四氯化碳密度比水大,己烷密度比水小;
④酸性越强,离子的结构质子的能力越弱.
解答:解:①同主族自上而下非金属性减弱,非金属性越强氢化物越稳定,故稳定性HF>HCl>HBr>HI,故①正确;
②电子层结构相同核电荷数越大离子半径越小,故离子半径F->Na+>Mg2+,故②错误;
③四氯化碳没得比水大,己烷密度比水小,故③错误;
④酸性碳酸>苯酚,水为中性,酸性越强,离子的结构质子的能力越弱,故结合质子能力:OH->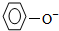 >HCO3-,故④正确;
>HCO3-,故④正确;
故选B.
②电子层结构相同核电荷数越大离子半径越小,故离子半径F->Na+>Mg2+,故②错误;
③四氯化碳没得比水大,己烷密度比水小,故③错误;
④酸性碳酸>苯酚,水为中性,酸性越强,离子的结构质子的能力越弱,故结合质子能力:OH->
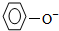 >HCO3-,故④正确;
>HCO3-,故④正确;故选B.
点评:本题考查同主族性质递变规律、半径比较、物质性质等,难度中等,注意基础知识的理解掌握.

练习册系列答案
相关题目
 >HCO3-.
>HCO3-.