题目内容
15.用电子式表示下列原子、阴阳离子、化合物(1)S
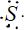 、Na
、Na 、K+K+、OH-
、K+K+、OH- 、Na2O2
、Na2O2 、NH4Cl
、NH4Cl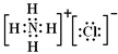
(2)电子式表示下列物质的形成过程HCl:
 、NaCl:
、NaCl: .
.
分析 (1)硫原子核外最外层有6个电子;钠原子最外层1个电子;钾离子电子式符号为阳离子符号;氢氧根离子带一个单位负电,氧原子与氢原子共用1对电子;过氧化钠为离子化合物,2个钠离子与过氧根离子通过离子键结合,两个氧原子之间共用1对电子;氯化铵为离子化合物,铵根离子与氯离子通过离子键结合,铵根离子内氮原子与氢原子之间通过共用电子对结合;
(2)氯化氢含有共价键,氢原子与氯原子共用1对电子;
氯化钠为离子化合物,钠离子与氯离子通过离子键结合.
解答 解:(1)硫原子核外最外层有6个电子,电子式为: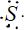 ;
;
钠原子最外层1个电子,电子式为: ;
;
钾离子电子式符号为阳离子符号:K+;
氢氧根离子带一个单位负电,氧原子与氢原子共用1对电子,电子式为: ;
;
过氧化钠为离子化合物,2个钠离子与过氧根离子通过离子键结合,两个氧原子之间共用1对电子,电子式: ;
;
氯化铵为离子化合物,铵根离子与氯离子通过离子键结合,铵根离子内氮原子与氢原子之间通过共用电子对结合,电子式: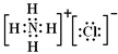 ;
;
故答案为: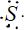 ;
; ;K+;
;K+; ;
; ;
;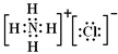 ;
;
(2)HCl为共价化合物,原子间以共用电子对成键,用电子式表示形成过程: ,
,
故答案为: ;
;
NaCl为离子化合物,用电子式表示形成过程为 ,
,
故答案为: .
.
点评 本题考查了电子式、用电子式表示离子化合物、共价化合物的形成过程,明确物质所含化学键类型是解题关键,题目难度不大.

练习册系列答案
相关题目
5.下列说法错误的是( )
| A. | 室温下,能将浓硫酸盛放在铁桶中 | |
| B. | NH4F溶液能存放于玻璃试剂瓶中 | |
| C. | 可燃冰主要是甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 | |
| D. | 可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
6.下列各组混合物中,能用分液漏斗进行分离的是( )
| A. | 酒精和水 | B. | 溴和CCl4 | C. | 水和苯 | D. | 汽油和植物油 |
3.一定能在下列溶液中大量共存的离子组是( )
| A. | AlCl3溶液:Na+、K+、SO42-、AlO2- | |
| B. | KW/c(OH-)=0.1mol/L的溶液:Na+、Mg2+、NO3-、S2- | |
| C. | 无色溶液:Na+、Ca2+、NO${\;}_{3}^{-}$、Cl- | |
| D. | 能使甲基橙呈黄色的溶液:H+、ClO-、Fe2+、Ag+ |
10.下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A. | 向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全: NH4++H++SO42-+Ba2++2OH-=NH3•H2O+BaSO4↓+H2O | |
| B. | Ca(HCO3)2溶液中加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+H2O | |
| C. | 用铜作电极电解饱和食盐水:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 以下有机物在碱性条件下水解的化学方程式: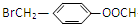 +3NaOH$\stackrel{△}{→}$ +3NaOH$\stackrel{△}{→}$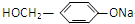 +HCOONa+NaBr +HCOONa+NaBr |
20.下列各组物质可按溶解、过滤、蒸发的操作顺序,将它们分离的是( )
| A. | 氧化铜和碳粉 | B. | 硝酸钾和硝酸钠 | C. | 水和酒精 | D. | 硫酸钠和硫酸钡 |
7.5.4gM和16.0gN恰好完全反应,生成0.2molX和10.2gY,则X的摩尔质量为( )
| A. | 28g•mol-1 | B. | 56g•mol-1 | C. | 84g•mol-1 | D. | 112g•mol-1 |
4.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 25℃,1.01×105 Pa,32 g O2和O3的混合气体所含原子数为2NA | |
| C. | 标准状况下,11.2LH2O 含有的分子数为0.5NA | |
| D. | 在常温常压下,44gCO2含有的分子数为3NA |
5.下列有关物质工业制法的反应原理错误的是( )
| A. | 侯氏制碱:NH3+CO2+H2O+NaCl=NH4Cl+NaHCO3↓ 2NaHCO3═Na2CO3+CO2↑+H2O | |
| B. | 氢氧化钠:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2NaOH | |
| C. | 高温下制粗硅:C+SiO2$\frac{\underline{\;高温\;}}{\;}$CO2↑+Si | |
| D. | 电解法制金属镁:MgCl2(熔融)$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑ |