��Ŀ����
����Ŀ����֪��AΪ���������ӵĵ���ɫ���廯���E��XΪ�����г������壬A��B��C��D������ͬ�Ľ������ӣ���ת����ϵ����ͼ�����ֲ��Z��ȥ)��
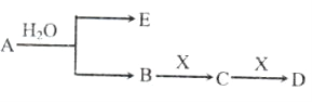
��ش���������:
��l�����ֽ������ӵ����ӽṹʾ��ͼΪ______��
��2��X�ĵ���ʽ______��
��3��B��������ѧ����������______�����³�ѹ�£�7.8g A��������ˮ��ַ�Ӧ�ų�����a kJ��д���÷�Ӧ���Ȼ�ѧ����ʽ______��
��4����CҲ��ת��ΪB��д����ת���Ļ�ѧ����ʽ______��
��B��D��Ӧ�����ӷ���ʽΪ______��
��5����һ����������Xͨ��2L B����Һ�У���������Һ�б���μ���ϡ����������������������������������ʵ����Ĺ�ϵ����ͼ������������ܽ��HCl�Ļӷ�����
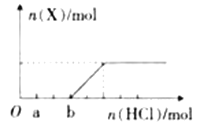
��ش�a����Һ���������ʵĻ�ѧʽΪ________��a-b֮��ķ�Ӧ�����ӷ���ʽ_____��
���𰸡� Na+ ![]()
![]() �����ԣ����ۼ������Ӽ� 2Na2O2(s)+2H2O(l)=4NaOH(aq)+O2(g) ��H=-20akJ/mol Ca(OH)2+ Na2CO3=CaCO3��+2NaOH ��Ba(OH)2+Na2CO3=BaCO3��+2NaOH OH-+HCO3-=CO32-+H2O Na2CO3��NaCl CO32-+H+=HCO3-
�����ԣ����ۼ������Ӽ� 2Na2O2(s)+2H2O(l)=4NaOH(aq)+O2(g) ��H=-20akJ/mol Ca(OH)2+ Na2CO3=CaCO3��+2NaOH ��Ba(OH)2+Na2CO3=BaCO3��+2NaOH OH-+HCO3-=CO32-+H2O Na2CO3��NaCl CO32-+H+=HCO3-
��������E��XΪ�����г������壬AΪ���������ӵĵ���ɫ���廯�������ˮ��Ӧ����E��B��Ӧ�ǹ���������ˮ��Ӧ����������������������AΪNa2O2��EΪO2��BΪNaOH��B��X����������Ӧ������֪XΪCO2��CΪNa2CO3��DΪNaHCO3��
(l)A�н�������ΪNa+�����ӽṹʾ��ͼΪ��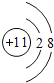 ���ʴ�Ϊ��
���ʴ�Ϊ��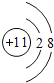 ��
��
(2)XΪCO2�������ʽΪ��![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��
(3)BΪNaOH���������Ӽ������ۼ������³�ѹ�£�7.8g Na2O2��������ˮ��ַ�Ӧ�ų�����akJ��2mol Na2O2��ȫ��Ӧ����ʽ������=a kJ��![]() =20a kJ����Ӧ���Ȼ�ѧ����ʽΪ��2Na2O2(s)+2H2O(l)=4NaOH(aq)+O2(g)��H=-20a kJ/mol���ʴ�Ϊ�����Ӽ������ۼ���2Na2O2(s)+2H2O(l)=4NaOH(aq)+O2(g)��H=-20a kJ/mol��
=20a kJ����Ӧ���Ȼ�ѧ����ʽΪ��2Na2O2(s)+2H2O(l)=4NaOH(aq)+O2(g)��H=-20a kJ/mol���ʴ�Ϊ�����Ӽ������ۼ���2Na2O2(s)+2H2O(l)=4NaOH(aq)+O2(g)��H=-20a kJ/mol��
(4)��̼����Ҳ��ת��Ϊ�������ƣ���ת���Ļ�ѧ����ʽΪ��Na2CO3+Ca(OH)2=CaCO3��+2NaOH���ʴ�Ϊ��Na2CO3+Ca(OH)2=CaCO3��+2NaOH��
������������̼�����Ʒ�Ӧ����̼������ˮ����Ӧ���ӷ���ʽΪ��HCO3-+OH-=CO32-+H2O���ʴ�Ϊ��HCO3-+OH-=CO32-+H2O��
(5)����Na2CO3+HCl=NaHCO3+NaCl��NaHCO3+HCl=NaCl+H2O+CO2��֪��Na2CO3ת��ΪNaHCO3��NaHCO3ת��ΪNaCl��Ҫ��HCl�����ʵ�����ȣ�ʵ���ϲ�������֮ǰ�������������������̼�����������֮��=3��2��������Һ�л�����NaOH��˵��ԭ��Һ��ΪNaOH��Na2CO3����Ϸ���ʽ��֪����Һ��n(NaOH)��n(Na2CO3)=1��2����a������������ǰ�������ᷴӦ̼����δ��Ӧ��a��ʱ��Һ�е�������Na2CO3��NaCl��b��ʱ��̼����ǡ��ת��Ϊ̼�����ƣ���a-b֮��ķ�Ӧ�����ӷ���ʽΪ��CO32-+H+=HCO3-���ʴ�Ϊ��Na2CO3��NaCl��CO32-+H+=HCO3-��


