题目内容
图3-21是金属钨晶体中的一个晶胞的结构示意图,它是一种体心立方结构。实验测得金属钨的密度为19.30 g·cm-3,钨的相对原子质量是183.9。假设金属钨原子为等径刚性球,试完成下列问题:
(1)每一个晶胞中分摊到__________个钨原子。
(2)计算晶胞的边长a。
(3)计算钨的原子半径r(提示:只有体对角线上的各个球才是彼此接触的)。

图3-21
(1)每一个晶胞中分摊到__________个钨原子。
(2)计算晶胞的边长a。
(3)计算钨的原子半径r(提示:只有体对角线上的各个球才是彼此接触的)。

图3-21
(1)2 (2)3.16×10-8 cm(3)1.37×10-8 cm
(1)正确应用分摊法确定一个晶胞中包含的各粒子的数目。
(2)应用基本关系式: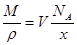 ,先求出晶胞的体积,然后根据V=a3计算晶胞边长。
,先求出晶胞的体积,然后根据V=a3计算晶胞边长。
(2)应用基本关系式:
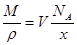 ,先求出晶胞的体积,然后根据V=a3计算晶胞边长。
,先求出晶胞的体积,然后根据V=a3计算晶胞边长。
练习册系列答案
相关题目