题目内容
【题目】![]() 溶液与
溶液与![]() 锌粉在量热计中充分反应。测得反应前温度为
锌粉在量热计中充分反应。测得反应前温度为![]() ,反应后最高温度为
,反应后最高温度为![]() 。
。
已知:反应前后,溶液的比热容均近似为![]() 、溶液的密度均近似为
、溶液的密度均近似为![]() ,忽略溶液体积、质量变化和金属吸收的热量。请计算:
,忽略溶液体积、质量变化和金属吸收的热量。请计算:
(1)反应放出的热量![]() _____J。
_____J。
(2)反应![]() 的
的![]() ______
______![]() (列式计算)。
(列式计算)。
【答案】![]()
![]()
【解析】
(1)根据中和滴定实验的原理可知,该反应放出的热量可根据Q=cm![]() 计算;
计算;
(2)结合焓变的概念及其与化学计量数之间的关系列式计算。
(1)100mL 0.200mol/L CuSO4溶液与1.95g锌粉发生反应的化学方程式为:CuSO4+Zn=ZnSO4+Cu,忽略溶液体积、质量变化可知,溶液的质量m=![]() =1.00g/cm3×100mL(cm3)=100g,忽略金属吸收的热量可知,反应放出的热量Q=cm
=1.00g/cm3×100mL(cm3)=100g,忽略金属吸收的热量可知,反应放出的热量Q=cm![]() =4.18
=4.18![]() ×100g×(30.1-20.1)
×100g×(30.1-20.1)![]() = 4.18×103J,故答案为:4.18×103;
= 4.18×103J,故答案为:4.18×103;
(2)上述反应中硫酸铜的物质的量n(CuSO4)= 0.200mol/L×0.100L=0.020mol,锌粉的物质的量n(Zn)=![]() =0.030mol,由此可知,锌粉过量。根据题干与第(1)问可知,转化0.020mol硫酸铜所放出的热量为4.18×103J,又因为该反应中焓变
=0.030mol,由此可知,锌粉过量。根据题干与第(1)问可知,转化0.020mol硫酸铜所放出的热量为4.18×103J,又因为该反应中焓变![]() 代表反应1mol硫酸铜参加反应放出的热量,单位为kJ/mol,则可列出计算式为:
代表反应1mol硫酸铜参加反应放出的热量,单位为kJ/mol,则可列出计算式为:![]() ,故答案为:
,故答案为:![]() (答案符合要求且合理即可)。
(答案符合要求且合理即可)。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案【题目】CdSnAs2是一种高迁移率的新型热电材料,回答下列问题:
(1)Sn为ⅣA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为_____________,其固体的晶体类型为_____________。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为_____________(填化学式,下同),还原性由强到弱的顺序为____________,键角由大到小的顺序为_____________。
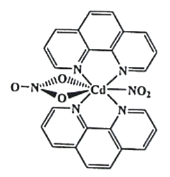
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种Cd2+配合物的结构如图所示,1mol该配合物中通过螯合作用形成的配位键有_________mol,该螯合物中N的杂化方式有__________种。
(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子的分数坐标。四方晶系CdSnAs2的晶胞结构如图所示,晶胞棱边夹角均为90°,晶胞中部分原子的分数坐标如下表所示。
坐标 原子 | x | y | z |
Cd | 0 | 0 | 0 |
Sn | 0 | 0 | 0.5 |
As | 0.25 | 0.25 | 0.125 |
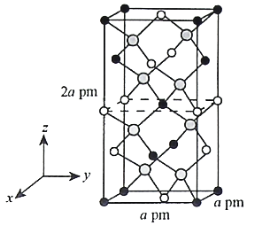
一个晶胞中有_________个Sn,找出距离Cd(0,0,0)最近的Sn_________(用分数坐标表示)。CdSnAs2
晶体中与单个Sn键合的As有___________个。